设为首页
设为首页
 加入收藏
加入收藏
教学设计方案一
课题:二氧化硫
教学重点:二氧化硫的化学性质
难点:二氧化硫的漂白作用
教学过程:
引入:我们知道硫在氧族中燃烧能够生成一种有刺激性气味气体二氧化硫。
播放视频:硫在氧气中燃烧。
引言:我们以硫为代表物,认识了氧族元素的主要化学性质,现在我们要学习硫的重要氧化物之一二氧化硫的性质、用途和危害。
讲述:物理性质
展示:闻气体气味正确方法的图片
演示实验:二氧化硫溶于水(此处若无演示条件,也可以播放视频文件)
讨论:根据二氧化硫的物质分类判断它是酸性氧化物,因此具有酸性氧化物的通性。
分析:二氧化硫与水反应的实验现象,既说明它能溶于水,又说明它和水反应生成了酸。在此可以复习可逆反应的概念。
讨论:二氧化硫溶于水的实验中为什么开始水面没有顺利上升?振荡后水面很快上升?(在液面上形成饱和亚硫酸溶液,阻止SO2的吸收。)
要求:学生写出证明二氧化硫是酸性氧化物的有关反应的化学方程式。
简介:亚硫酸
讨论:根据二氧化硫中硫元素的化合价推断它应具有的化学性质。
讲述:当二氧化硫遇到强还原剂时,表现出氧化性。例如:二氧化硫和硫化氢反应可以生成硫和水。
过渡:二氧化硫主要表现出还原性。
讲述:二氧化硫和氧气的反应
增加演示实验:二氧化硫使碘水褪色。
分析:此实验说明了什么?由此推断二氧化硫能否使高锰酸钾溶液褪色,使氯水、溴水褪色?写出有关反应的化学方程式。
演示实验:二氧化硫使品红溶液褪色。
分析:二氧化硫的漂白原理并与氯气等作对比,小结具有漂白性的物质。
讨论:根据二氧化硫的性质推断它的用途。
过渡:二氧化硫在工业上可以作漂白剂,还能杀灭霉菌和细菌,作食物和干果的防腐剂。但是也有不法之徒利用二氧化硫的性质,让馒头、银耳变得更白,只顾个人利益,不管他人的身体健康。请同学们今后要注意。此外,二氧化硫还是污染大气的主要有害物质之一。
讲述:二氧化硫的污染。酸雨的概念和危害。
展示图片、播放有关酸雨的录像。
小结:
作业:写出鉴别二氧化硫和二氧化碳的方法。
板书设计:
第二节 二氧化硫
一、二氧化硫的性质
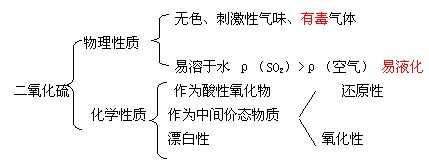
1.物理性质
无色、有毒、刺激性气味的气体;易液化、易溶于水(1 :40)
2.化学性质
(1)具有酸性氧化物的通性
![]()
![]()
![]() (可逆反应);
(可逆反应);
![]() ;
;
![]() ;
;
![]() (
( ![]() 过量)
过量)
![]()
![]()
![]()
![]()
![]()
![]()
(2)二氧化硫的氧化还原反应
①弱氧化性: ![]()
![]()
![]()
②较强的还原性:
如 ![]() 能使氯水、溴水、
能使氯水、溴水、 ![]() 溶液褪色。
溶液褪色。
![]()
![]()
![]()
![]() (与
(与 ![]() 有类似反应)
有类似反应)
* ![]() (此方程式不要求学生掌握)
(此方程式不要求学生掌握)
(3)漂白性
3.用途
二、二氧化硫的污染
酸雨
教学设计方案二
课题:二氧化硫
教学重、难点:二氧化硫的化学性质。
教学过程:
资料引入:[投影 1]
1、1872年,美国化学家Smith,首先提出了“酸雨”一词,直到本世纪四十年代,酸雨问题才引起人们的广泛关注。
2、1972年6月5日,具有历史意义的人类环境会议在瑞典首都斯德哥尔摩召开,通过了著名的《人类环境宣言》,并确定每年6月5日为“世界环境日”。从1974年起,每年由联合国环境规划署确定一个主题,开展“世界环境日”的活动,其中1983年的主题是防治酸雨。
3、1985年,几场酸雨过后,我国四川奉节县9万亩华山松全部枯死,重庆南山2.7万亩马尾松死亡过半。
提出问题:酸雨的危害如此之大,造成酸雨的罪魁祸首是谁呢?――是二氧化硫,今天我们共同讨论关于二氧化硫的问题。
教师板书:
第二节 二氧化硫
演示实验:收集一试管二氧化硫气体,将其倒置在水槽中,晃动试管。
学生活动:观察SO2气体的颜色、状态;闻气体的气味;分析SO2的水溶性。
教师引导:二氧化硫的其它物理性质如何?请同学结合已有知识,阅读课本158页第二段。
学生活动:略。
教师板书:

教师引导:二氧化硫溶于水后是否与水反应?
演示实验:将充有水的试管倒立过来,向其中滴入几滴紫色石蕊试液。
学生活动:观察、分析实验现象。书写相应的化学方程式。
教师板书: 化学性质
教师引导:看来,作为酸性氧化物来说,SO2可以与水作用,生成亚硫酸。但亚硫酸不稳定,容易分解,请同学书写有关化学方程式。
教师引导:我们把两个化学方程式放在一起观察,你发现什么?
学生活动:是可逆反应。符合条件:同时、同条件。
教师引导:看来化学方程式应写为:SO2
+ H2O ![]() H2SO3(学生完成)作为酸性氧化物,除了和水反应,生成相应的酸外,还可以和哪类物质反应?
H2SO3(学生完成)作为酸性氧化物,除了和水反应,生成相应的酸外,还可以和哪类物质反应?
学生回答:碱。
教师引导:了解二氧化硫的这些性质后,请同学讨论如何收集二氧化硫?
学生讨论:侧重易溶于水、比空气重、有毒三个方面。
教师小结:向上排空气法,用蓝色石蕊试纸检验,同时配上NaOH溶液尾气吸收。刚才我们讨论的反应,化合价前后没有发生变化,请同学标出SO2中硫元素的化合价,分析可能具有什么样的性质?
教师板书:

教师引导:[录 像]二氧化硫和氧气反应的实验。请同学写出反应的化学方程式。分析二氧化硫在此处作氧化剂还是还原剂?
学生活动: 还原性
2SO2 +
O2 ![]() SO3
SO3
教师设问:如果2molSO2 与1molO2在上述条件下充分反应,能否得到2molSO3?
教师过渡:生成的SO3为无色固体,和SO2在性质上有明显不同,但它们都是酸性氧化物,都能溶与水生成相应的酸。SO2作为氧化剂,又能发生什么样的反应?请同学推测SO2和H2S反应的生成物,尝试写出反应的化学方程式,并分析电子得失状况。
教师引导:我们刚刚讲过的O3,还有HClO、Na2O2等都是强氧化剂,具有漂白性;SO2氧化性较弱,能漂白吗?
演示实验:[实验6-2]
教师引导:能漂白,但不持久(而O3
、HClO、Na2O2的漂白具有永久性)看来它们的作用原理不同。SO2不是氧化性漂白,仅仅是SO2与有色物质结合生成不稳定的无色物质,同时又容易分解,恢复原来有色物质的颜色。
教师板书: 漂白性
教师引导:SO2在日常生活中有一定用处,但它的危害性也非同小可(出示云岗石窟明信片)。山西是产煤大省,空气中SO2含量超标。请同学利用所学知识,讨论如何回收SO2,防止大气污染?(先阅读160页有关内容,再进行讨论)
教师结课:望大家在未来的环保工作中大显身手。
布置作业:161页一题、二题、三题。
板书设计: