 设为首页
设为首页
 加入收藏
加入收藏
教学设计方案一
课题:盐类的水解
重点:理解盐类水解的本质
难点:盐类水解方程式的书写和分析
第一课时
教学设计
1.采用实验手段启发学生思考,激发学生学习兴趣,调动学生学习积极性。(此实验可在教师指导下由学生完成)
(1)用蒸馏水配制 ![]() 溶液,
溶液, ![]() 溶液,
溶液, ![]() 溶液。
溶液。
(2)用 ![]() 试纸测定三种盐溶液的
试纸测定三种盐溶液的 ![]() ,并记录:
,并记录:
![]()
![]()
![]()
![]() :
:
教师设疑:(1)为什么三种盐的水溶液有的呈中性?有的呈碱性?有的呈酸性呢?
(2)同呈中性的 ![]() 和
和 ![]() 其实质是否相同呢?
其实质是否相同呢?
2.盐类水解实质
教师通过对强碱弱酸所生成盐的水解的分析,引导学生思考并讨论强酸和弱碱所生成盐的水解。
教师引导学生进行归纳:
盐溶液是碱性,溶液中 ![]() 增大?为什么会增大呢?
增大?为什么会增大呢? ![]() 是从哪来的呢?
是从哪来的呢?
盐溶液呈酸性,溶液中 ![]() 增大?为什么会增大呢?
增大?为什么会增大呢? ![]() 是从哪来的呢?
是从哪来的呢?
3.引导归纳盐组成与其水解和溶液酸碱性的内在联系。
教学步骤
(一)知识准备
酸+碱=盐+水(中和反应,可以理解盐可以由相应的酸和碱反应生成)

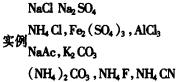
(二)引入新课
1.准备四种盐溶液。分别测定它们
![]() 。并作记录:
。并作记录:
![]() 溶液酸碱性分析
溶液酸碱性分析
(1) ![]() 溶液。
溶液。
(2) ![]() 溶液。
溶液。
(3) ![]() 溶液。
溶液。
(4) ![]() 溶液。
溶液。
2.根据现象引导思考:
(1)盐溶液是否一定都呈中性?从实验现象你认为哪些盐溶液可呈中性?
(2)为什么盐溶液有的呈酸性,有的呈碱性呢?
(3)同呈中性的 ![]() 和
和 ![]() 其实质是否相同呢?
其实质是否相同呢?
3.点题
本节讨论的盐类水解知识帮助我们来解决这些问题。
(1)盐类水解实质:
① ![]() 溶液(弱碱强酸盐,水溶液
溶液(弱碱强酸盐,水溶液 ![]() ,呈酸性)
,呈酸性)
![]() (盐电离强电解质电离是完全的)
(盐电离强电解质电离是完全的)
![]()
![]()
![]() (水电离,弱电解电离是部分的,可逆的)
(水电离,弱电解电离是部分的,可逆的)
![]()
![]()
![]() 由于生成难电离的弱电解质
由于生成难电离的弱电解质
![]() 促使水的电离,使溶液中
促使水的电离,使溶液中 ![]() 增大,从而使溶液呈酸性。
增大,从而使溶液呈酸性。
水解方程式: ![]()
![]()
![]()
水解离子方程式: ![]()
![]()
![]()
② ![]() 溶液(强碱弱酸盐,水溶液
溶液(强碱弱酸盐,水溶液 ![]() ,呈碱性)
,呈碱性)
![]() (盐,弱电解质,完全电离)
(盐,弱电解质,完全电离)
![]()
![]()
![]() (水,弱电解质,存在电离平衡)
(水,弱电解质,存在电离平衡)
![]()
![]()
![]() 由于生成难电离的弱电解质
由于生成难电离的弱电解质
![]() 分子,使溶液中
分子,使溶液中 ![]() 减少,促使
减少,促使 ![]() 的电离,从而使溶液中
的电离,从而使溶液中 ![]() 增大,溶液呈现碱性。
增大,溶液呈现碱性。
③ ![]() 溶液
溶液
![]() (盐,强电解质,完全电离)
(盐,强电解质,完全电离)
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 由于
由于 ![]() 结合
结合 ![]() 的能力与
的能力与 ![]() 的能力相当,使溶液中
的能力相当,使溶液中 ![]() 与
与 ![]() 仍相等,所以溶液呈中性。
仍相等,所以溶液呈中性。
(三)随堂练习
1.在水中加入下列物质,可使水的电离平衡向电离方向移动的是( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
2.判断下列盐类水解的叙述中正确的是( )
A.溶液呈中性的盐一定是强酸、强碱生成的盐
B.含有弱酸根盐的水溶液一定呈碱性
C.盐溶液的酸脓性主要决定于形成盐的酸和碱的相对强弱
D.碳酸溶液中氢离子物质的量浓度是碳酸根离子物质的量浓度的两倍
3.物质的量浓度相同的下列溶液中,含微粒种类最多的是( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
4.下列各组离子,在强碱性溶液中可以大量共存的是( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
5.为了使 ![]() 溶液中
溶液中 ![]() 的比值变小,可加入的物质是( )
的比值变小,可加入的物质是( )
A.适量盐酸 B.适量 ![]() 溶液
溶液
C.适量KOH溶液 D.适量KHS溶液
(四)总结、扩展
1.盐类水解的实质
在溶液中,由于盐的离子与水电离出来的 ![]() 和
和 ![]() 生成弱电解质,从而破坏水的电离平衡,使溶液显示出不同程度的酸性、碱性或中性。
生成弱电解质,从而破坏水的电离平衡,使溶液显示出不同程度的酸性、碱性或中性。
2.盐类水解的类型和规律
(1)通常盐类水解程度是很小的,而且是可逆的。
(2)水解规律:
有弱才水解,无弱不水解,越弱越水解,都弱都水解;谁强显谁性,同强显中性。
①强酸弱碱生成的盐水解:溶液呈酸性,是弱碱的阳离子水解生成对应的弱碱,使溶液显酸性。如: ![]() 等。
等。
②强碱弱酸生成的盐水解,溶液呈碱性,原因是弱酸根发生水解,生成对应弱酸,使溶液显碱性,如: ![]() 等。
等。
③强酸强碱盐不水解,溶液呈中性,如 ![]() 等。
等。
④弱酸弱碱盐强烈水解。(此内容大纲不作要求,不宜向学生补充)
a.酸强于碱,显酸性,如 ![]() ;
;
b.碱强于酸,显碱性,如 ![]()
c.酸碱相当,显中性,如 ![]()
⑤弱酸酸式盐水解:取决于酸式酸根的电离程度和水解程度相对大小。
a.若电离程度大于水解程度,溶液呈酸性,如 ![]() 等。
等。
b.若电离程度小于水解程度,溶液呈碱性,如 ![]() 等。
等。
3.扩展
氮、磷、钾是植物生长的重要营养元素,洗衣粉中加入由磷酸脱水制得的多磷酸的钠盐作配料,能起到软化水的作用,但使用此类洗衣粉会造成水质污染。
(1)试简述污染水质的原因。
(2)某种无磷洗衣粉中加入了硅酸钠作配料,试说明这种配料的有关性质和作用。
板书设计
一、盐的组成类别
1.强酸强碱盐:如
![]() 等;
等;
2.强酸弱碱盐:如
![]() 等;
等;
3.弱酸弱碱盐:如
![]() 等;
等;
4.弱酸弱碱盐:如
![]() 等;
等;
二、实验测定盐溶液的 ![]() 是不是都等于7
是不是都等于7
1.测蒸馏水 ![]() ;
;
2.测 ![]() 溶液
溶液 ![]() ;
;
3.测 ![]() 溶液
溶液 ![]() ;
;
4.测 ![]() 溶液
溶液 ![]() 值。
值。
列表比较:
提出问题:为什么都是盐溶液的(2)(3)(4)三种溶液 ![]() 会有显著差异呢?
会有显著差异呢?
![]() :强酸强碱盐
:强酸强碱盐 ![]() ;
;
![]() :强碱弱酸盐
:强碱弱酸盐 ![]() ;
;
![]() :强碱强酸盐
:强碱强酸盐 ![]() ;
;
剖析原因:写出离子方程式及化学方程式。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 与
与 ![]() 电离出来
电离出来 ![]() 结合成弱电解质
结合成弱电解质 ![]()
![]()
![]()
![]() 破坏了水电离平衡,减少水电离,使溶液中
破坏了水电离平衡,减少水电离,使溶液中
![]() 浓度增大,碱性增强。
浓度增大,碱性增强。
![]()
![]()
![]()
![]()
![]()
![]()
![]() 与
与 ![]() 电离出来的
电离出来的 ![]() 结合生成弱碱
结合生成弱碱 ![]() ,破坏了水电离平衡,促使水电离,使溶液中
,破坏了水电离平衡,促使水电离,使溶液中 ![]() 浓度增大,酸性增强。
浓度增大,酸性增强。
![]() 强酸、强碱盐,不水解只电离。溶液显中性。
强酸、强碱盐,不水解只电离。溶液显中性。
三、引出水解定义,归纳水解一般规律
1.定义:在溶液中盐电离出来的离子跟水电离出来的
![]() 或
或 ![]() 结合生成弱电解质的反应叫做盐类水解。
结合生成弱电解质的反应叫做盐类水解。
2.水解一般规律:
谁弱谁水解:水解离子一定是盐电离出来的弱离子(弱酸阴离子,或弱碱阳离子)。
谁强显谁性:碱强显碱性,酸强显酸性。
都强不水解。
都弱都水解(了解就可)
教学设计方案二
第二课时
目标:
1.影响盐类水解的因素,与水解平衡移动。
2.盐类水解的应用。
教学设计:
1.师生共同复习巩固第一课时相关知识。
(1)根据盐类水解规律分析
醋酸钾溶液呈 性,原因 ;
氯化铝溶液呈 性,原因 ;
(2)下列盐溶于水高于浓度增大的是
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
2.应用实验手段,启发思维
实验1.在溶液中滴加几滴酚酞试液,观察现象,分析为什么?将溶液分成二等份装入二支干净试管中,一支加热,另一支保持室温,进行比较。
现象 ;
原因分析 ;
实验2.将新制备的 ![]() 胶体中,分装于二支试管中,一支试管加入一滴盐酸,与另一支试管对照比较。
胶体中,分装于二支试管中,一支试管加入一滴盐酸,与另一支试管对照比较。
现象 ;
原因分析 。
教学过程:
影响盐类水解的因素
1.主要因素是盐本身的性质。
组成盐的酸根对应的酸越弱,水解程度也越大,碱性就越强, ![]() 越高。
越高。
组成盐的阳离子对应的碱越弱,水解程度也越大,酸性就越强, ![]() 越低。
越低。
2.影响盐类水解的外界因素主要有温度、浓度及外加酸碱等因素。
(1)温度:盐的水解是吸热反应,因此升高温度水解程度增大。
(2)浓度:盐浓度越小,水解程度越大;
盐浓度越大,水解程度越小。
(3)外加酸碱能促进或抑制盐的水解。例如水解呈酸性的盐溶液加入碱,就会中和溶液中的 ![]() ,使平衡向水解方向移动而促使水解,若加酸则抑制水解。
,使平衡向水解方向移动而促使水解,若加酸则抑制水解。
盐类水解知识的应用
1.盐溶液的酸碱性判断
根据盐的组成及水解规律分析。“谁弱谁水解,谁强显谁性”作为常规判断依据。
例题:分析: ![]() 溶液是显酸性?还是显碱性?为什么?
溶液是显酸性?还是显碱性?为什么?
分析: ![]() 溶液是显酸性?还是显碱性?为什么?
溶液是显酸性?还是显碱性?为什么?
2.比较溶液中酸碱性的相对强弱。“越弱越水解”
例题:分析 ![]() 溶液与
溶液与 ![]() 溶液的碱性强弱?
溶液的碱性强弱?
∵ ![]() 的酸性比
的酸性比 ![]() 酸性强。
酸性强。
∴ ![]() 水解程度大于
水解程度大于 ![]() 水解程度。
水解程度。
∴
![]() 溶液碱性强于
溶液碱性强于 ![]() 溶液碱性。
溶液碱性。
3.溶液中离子浓度大小的比较
电解质水溶液K存在着离子和分子,它们之间存在着一些定量关系。也存在量的大小关系。
(1)大小比较:
①多元弱酸溶液,根据多元酸分步电离,且越来越难电离分析。如:在 ![]() 溶液中,
溶液中,![]() ;
;
②多元弱酸正盐溶液,根据弱酸根分步水解分析。如:在 ![]() 溶液
溶液
中,![]() ;
;
③不同溶液中同一离子浓度的比较要看溶液中其他离子对其影响因素。
④混合溶液中各离子浓度比较,要进行综合分析,要考虑电离、水解等因素。
(2)定量关系(恒等式关系)
①应用“电荷守恒”分析:
电解质溶液呈电中性,即溶液中阳离子所带正电荷总数与阴离子所带负电荷总数相等。如 ![]() 溶液中,阳离子有
溶液中,阳离子有 ![]() 和
和 ![]() ,阴离子有
,阴离子有 ![]() ,
, ![]() ,
, ![]() ,根据电荷守恒原理有:
,根据电荷守恒原理有: ![]()
②应用“物料守恒”方法分析。
电解质溶液中某一组份的原始浓度(起始浓度) ![]() 应等于它在溶液中各种存在形式的浓度之和。如:晶体
应等于它在溶液中各种存在形式的浓度之和。如:晶体 ![]() 中,
中, ![]()
在 ![]() 溶液中:
溶液中: ![]()
例题分析:
在 ![]() 溶液中存在的下列关系中不正确的是:
溶液中存在的下列关系中不正确的是:
A. ![]()
B. ![]()
C. ![]()
D. ![]()
解题思路:
溶液中存在二个守恒关系
a.电荷守恒,即
![]() …………(1)
…………(1)
b.物料守恒,即晶体中:
![]()
在溶液中S元素存在形式有三种: ![]() ,
, ![]() 及
及 ![]()
∴ ![]() ………………(2)
………………(2)
将(2)-(1)得
![]()
综上分析,关系正确的有A.C.D。答案:[B]
随堂练习
1.在 ![]() 溶液中存在的下列关系不正确的是( )
溶液中存在的下列关系不正确的是( )
A. ![]()
B. ![]()
C. ![]()
D. ![]()
2.为了除去 ![]() 酸性溶液中的
酸性溶液中的 ![]() ,可在加热搅拌下加入一种试剂过滤后,再加入适量盐酸,这种试剂是( )
,可在加热搅拌下加入一种试剂过滤后,再加入适量盐酸,这种试剂是( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
3.下列各物质中,指定微粒的物质的量为1:1的是( )
A. ![]() 中的
中的 ![]() 和
和 ![]() B.
B. ![]() 的纯水中
的纯水中 ![]() 和
和 ![]()
C. ![]() 中电子和中子 D.明矾溶液中
中电子和中子 D.明矾溶液中 ![]() 与
与 ![]()
4.下列溶液加热蒸干后,不能析出溶质固体的是( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
总结、扩展
1.影响盐类水解的因素及其影响原理。
2.盐类水解知识的应用:
(1)配制某些盐溶液,如配制澄清 ![]() 溶液。
溶液。
(2)除去溶液中某些杂质离子。如除去 ![]() 溶液中混有的
溶液中混有的 ![]() 。
。
3.扩展
泡沫灭火剂包括 ![]() 溶液(约1mol/L),
溶液(约1mol/L), ![]() 溶液(约1mol/L)及起泡剂。使用时发生的化学反应方程式是
。
溶液(约1mol/L)及起泡剂。使用时发生的化学反应方程式是
。 ![]() 溶液和
溶液和 ![]() 溶液的体积比约是 。若用等体积、等浓度的
溶液的体积比约是 。若用等体积、等浓度的
![]() 溶液代替
溶液代替 ![]() 溶液,在使用时喷不出泡沫,这是因为
;若用固体
溶液,在使用时喷不出泡沫,这是因为
;若用固体 ![]() 代替
代替 ![]() 溶液,在使用时也喷不出泡沫,这是因为
。泡沫灭火器内的玻璃筒里盛硫酸铝溶液,铁筒里盛碳酸氢钠溶液,不能把硫酸铝溶液盛在铁筒里的原因是
。
溶液,在使用时也喷不出泡沫,这是因为
。泡沫灭火器内的玻璃筒里盛硫酸铝溶液,铁筒里盛碳酸氢钠溶液,不能把硫酸铝溶液盛在铁筒里的原因是
。
板书设计:
1.水解的一般规律
(1)谁弱谁“水解”,谁强显谁“性”,可作为盐溶液性质(酸性或碱性)的常规分析方法。
(2)越弱越水解。
①碱越弱,对应阳离子水解程度越大,溶液酸性越强,对应弱碱阳离子浓度越小。
②酸越弱,酸根阴离子水解程度越大,溶液碱性越强,对应酸根离子浓度越小。
(3)水解是微弱的。
(4)都强不水解。
2.外界条件对盐水解的影响
(1)温度(实验1)
(2)溶液的酸、碱性(实验2)
3.盐类水解利用
(1)应用水解知识,配制某些盐溶液。如配制澄清 ![]() 溶液。方法:加酸(
溶液。方法:加酸( ![]() ),抑制
),抑制 ![]() 水解。
水解。
(2)除去溶液中某些杂质离子:如 ![]() 溶液中混有杂质
溶液中混有杂质 ![]() 。方法:加热,促使
。方法:加热,促使 ![]() 水解,使生成
水解,使生成 ![]() 除去。
除去。
4.典型例题
5.扩展