 设为首页
设为首页
 加入收藏
加入收藏
教学设计示例二
【教学目标】
1、日常生活中常见的干电池入手,首先对这些电池及拆解,了解其基本结构,通过网络资源,了解干电池中各化学物质的基本功能,为学习原电池的原理作准备;
2、使学生掌握原电池的基本化学原理;
3、通过原电池的教学活动,培养学生分析问题和解决问题的能力,并进行对立统一规律的辩证唯物主义教育;
4、以小组为单位,布置学习任务,组员分工协作,培养学生团结协作的团队精神;
5、由学生介绍日常生活中常见的各种干电池,以及当今电池发展概况,以及废旧电池回收的意义,增强学生的环境保护意识。展示各组对废旧电池回收后,作出各种无公害处理、有回收价值的化学原料的回收利用的可行性分析报告。
【教学重点】
原电池的基本化学原理
【教学难点】
1、原电池的基本化学原理;
2、原电池电极的判断及电极反应式。
【教学用具】
电流计、烧杯、导线(带鳄鱼嘴)、视频展示台、大屏幕投影多媒体计算机等。
![]()
锌板、铁板、铜板、石墨电极、常见品牌的碳性电池、碱性电池、锂离子电池、铅-酸蓄电池等。
【教学过程】
(引入) 日常生活中,我们会接触到不同种类的电池,有一次性的锌-锰酸性电池,有可重复充电的镍氢、镍镉电池、铅酸电池、锂离子电池等。这些电池虽小,但是,在生活中却扮演着及其重要的角色。你们知道电池工作的基本原理吗?它是如何发展、演化的呢?今天,我们来学习新的知识──原电池。
(展示样品)
(学生活动)
1、以组为单位,分别介绍本组课前拆解干电池的分析报告,通过查阅资料,所获取各个方面的信息。
2、分组介绍本组在获取感性知识的过程中,对电池工作原理的初步推测。
一、原电池的原理:
(提问)
将一块锌片投入稀硫酸中,会有什么现象?
(产生无色气体,同时放出热量)
锌与稀硫酸反应的实质是什么?
![]()
(结论)
锌与稀硫酸反应是一个氧化还原反应,锌失去电子,被氧化,溶液中的氢离子得到电子,被还原。这是一个化学反应完成的两个方面,没有锌失电子,就不存在在铜板上氢离子得到电子,氧化反应、还原反应同时进行,同生共灭并相互依存。从反应过程中放出热量的角度来说,这个反应将化学能转化为热能。
(提出假设)
在自然界中存在着能量守恒,能量可以从一种形式转化为另一种形式,我们能否充分利用这些能量呢?
如果将锌与稀硫酸的反应分两步完成,即:第一步锌失电子变为锌离子;第二步氢离子得电子,转化为氢原子,形成氢气。而电子的转移人为加以控制,此过程是否可行?如何实现?
(小组讨论) 上述假设能否通过实验手段实现?
(演示实验-1)
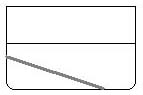
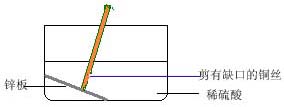
锌片与稀硫酸反应 在反应体系中插入一特制铜丝
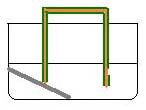
将特制的铜丝变形
(演示实验-2)
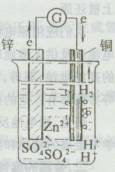
1.将一块锌板放入稀硫酸中;
2.将一块铜板放入稀硫酸中;
3.将锌板与铜板用导线相连;
4.将电解质溶液锌板、铜板、导线、电流计、组成回路。
通过实验可以看出在闭合回路中有电流流过,因此,实现了化学能转化为电能。
(结论)原电池的定义:将化学能转化为电能的装置叫做原电池。
(提问、讨论)①电流形成的条件?
(1.电荷的定向移动;2. 闭合回路,存在电动势)
②怎样构造闭合回路?
(电极、连接导线、电解质溶液……)
① 电动势是如何产生的呢?
(计算机辅助教学)
从微观角度进行分析。
(小结)
构成原电池的条件:
①活动性不同的两电极,且两电极由导线相连;
②电解质溶液,且两电极浸入其中。
(板书)
1. 构成原电池的条件:
①活动性不同的电极,且两电极由导线相连;
②电解质溶液,且两电极浸入其中。
(提问、讨论)
①原电池已经形成,如何判定它的正负极呢?
(电子流出的是负极,电子流入的为正极)
②判断下列原电池的正负极,并说明原因。
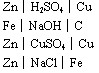
(实验)
学生自己用电流计加以验证。
(小结)
原电池的正、负极的判断。
(板书)
2. 原电池的正、负极的判断。
在原电池中,较活泼的金属作负极,较不活泼的金属或石墨电极作正极。
(讨论)
影响原电池的电动势大小的最主要的因素是什么?
(构成正、负电极的材料活泼性差异。差异大,电动势大。)
(讲述) 电极上发生的化学反应及表示方法。

(结论)原电池是以氧化还原反应为依据,使氧化反应与还原反应分别在设置的两个电极上进行,从而产生电流的装置。
(讲述)在科学技术飞速发展的今天,新材料、新能源成为各国高科技领域重要研究课题。利用原电池原理制得的各种新型电池不断涌现,电池向体积小、质量轻、可重复充电、高容量发展。但制造电池的过程中都用到一些重金属,例如:锰、镉、汞等,如果废旧电池随便丢弃,这些重金属离子泄漏会造成环境污染,而这种固体无机废弃物的污染很难治理,并且会影响几十年以至上百年,回收废旧电池根本在于合理科学地处理,并把有用的物质加以回收,希望我们同学从自己做起,保护环境,人人有责。
(展示)
1.常见干电池中的化学物质可能对环境造成那些影响?
2.各小组对常见干电池中的化学物质的回收、再利用、进行可行性分析。
3.各小组展示本组提出的旧干电池回收再利用的流程。
4.对各组所提方案进行评价。
(总结)
1. 构成原电池的条件;
2. 原电池正、负极的判断;
3. 电极反应表示方法。
(反馈)
1. 实验室制取氢气,用锌与稀硫酸反应。锌用纯锌好,还是用粗锌好(杂质为碳)?为什么?
2. 实验室只有纯的锌粒,怎么办?
附:板书计划
§3-6 原电池
一、原电池的原理:
1. 构成原电池的条件:
①金属活动性不同的电极,且两电极由导线相连;
②电解质溶液,且两电极浸入其中。
2.原电池的正、负极的判断。
在原电池中,较活泼的金属作负极,
较不活泼的金属或石墨电极作正极。
3.电极反应的表示法:
