 ��Ϊ��ҳ
��Ϊ��ҳ
 �����ղ�
�����ղ�
�̲ķ���
�����̲���Ҫ�ֳ������֣��������������ӵļ��顣��ɽ̲���ȣ��½̲��а���������Ϊѡѧ���ݣ�ͻ�����ڵ��ص����ݡ�
��������ѧ���ڳ����Ѿ��Ӵ������ᣬѧ��ϡ��������ʡ���˽̲Ŀ�ʼ�Ծ�֪ʶ���롣������ǿ����ʣ���ϰϡ��������ʡ�Ȼ��ת������������˾������ͨ�����һЩ���ԡ������ᡢŨ���ᡢϡ���ᣬ�����������������ɴ��С�����䣬�����Һ�����ӵ��ʵı仯��
��������Ⱦ������ͨ�ԣ��־���һ�������ԡ�ϡ������Ҫ��ʾ���ԣ���Ũ���ỹ������ˮ�ԡ���ˮ�Ժ�ǿ�����ԡ����Dz���˵ֻ��Ũ����ž��������ԣ�ϡ����Ҳ�������ԣ�ֻ�DZȽ������������������ϡ�
����Ũ�������ˮ�Ժ���ˮ���Dz�ͬ���������������ˮ�ԣ�ѧ�������Ѿ�ѧ������˽̲���Ҫ��������ˮ�ԣ���ͨ��ʵ�����˵����
����Ũ������������DZ��ڵ��ص����ݣ�Ҳ��һ���ѵ㡣�̲�ͨ��ʵ����ѧ���۲죬Ȼ��ó����ۡ����ݷ�Ӧ������������ʹ��ɫʯ����Һ������ʹƷ����Һ��ɫ��ѧ�����Ժܿ���֪���������Ƕ��������ɴ�˵��Ũ�����������Ӧһ�㲻�ų��������˷�Ӧ����������ԭ��Ӧ��Ȼ���ٸ���ϡ�ͺ���ҺΪ��ɫ����֪�˷�Ӧ����������ͭ������ѧ�������Լ���ɷ�Ӧ�Ļ�ѧ����ʽ��������Ӧǰ��Ԫ�ػ��ϼ۵ı仯�����Ժ����ó�Ũ�������ǿ�����ԵĽ��ۡ�����ͨ��ѧ���۲�ʵ�飬����ʵ�����ó����۵ķ�ʽ���֪ʶ������ѧ������֪���ɣ��ܺõĽ����ѧ����֪ʶ�������н�һ������ߡ�
���������������;���̲�ͨ��ͼʾ����ʽ�����˵ĸ�������ʦ������ѧ�����������������۹��ɳ���;�������ʦҲ�����ʵ������ҹ����Ṥҵ��չ����״�����ϣ�������ʵ�ʽ��������
����������������Ӽ�����һ���֣��̲IJ�ȡ��ϰ����֪ʶ���۲�ʵ�顢��¼������ԭ�ó����ۡ�
�������ڰ����������ε�ѡѧ���ݡ�
�������ڽ�ѧ�ص㣺Ũ��������ʺ���������ӵļ��顣
�����ѵ㣺Ũ����������ԡ�
�����������ʵĽ�ѧ����
�������Բ�ȡչʾʵ���ѧ���Լ�̽�����ܽ�ó����ʵ��������ʡ����磺
����չʾ��Ũ���ᣨ��ƿ����
������һѧ�����Լ�ƿ����������״Һ�塣
������ʾ��������ƽһ�߷�����Ũ���ᣬ��һ�߷Ű�ƿŨ���ᣨ�ݻ���ͬ����
����ѧ�������������ܶȴ�
������ʾ���ֱ��Ũ�����Ũ�����ƿ����������
����ѧ�������������ѻӷ�����Ũ������Ƚϵó�����
������ʾ����ʢ��ˮ���ձ�����������Ũ���Ტ���Ͻ��衣
����ѧ�����������������������ˮ���ܣ����ų��������ȡ�
������������ѧ���������У���Ȥ��Ȼ��˼ά������Ծ����ʵ���ϸ�ѧ�������ˡ����֡����龳����ѧ��ͨ��̽��������������������ʣ���ӡ����̡�
������ļ�����������
����ѧ���ӳ��нӴ���ѧ�����˽��˺ܶ����������ʡ�������ѧϰ�����в������⣬���磺������������Ժ������������ֲ���������ǿ�����жϲ���ȷ�ȡ���ʦӦ�ü�ʱ����ѧ������С�ᡣ�������ý����������ݣ������֪ʶ���б�����
һ��������������������
��������������ָ������������ԡ����磺Ũ���ᣨH2SO4�������ᣨHNO3���������ᣨHMnO4�����ظ��ᣨH2Cr2O7���������ᣨHClO���ȡ�
�����κ����ˮ��Һ�ܵ����H���������������ԣ�����������ᶼ�������ԡ�
�����ӷ������벻�ӷ�����
�����ӷ�������ᡢ�����ᡢ���ᡢ�����ᡢ������
�������ӷ�������ᡢ���ᡢ����
��������ǿ�����жϣ�
����ǿ�HClO4��HI��HNO3��HCl��H2SO4
������ǿ�H2SO3>
H3PO4>HNO2
�������HF>CH3COOH
> H2CO3 >
H2S > HClO > HCN >
H2SiO3
�ġ�����
����������������Ϊ�����������N2O5��SO3�ȡ�
Ũ���� �� ϡ����
����ϡ�����������ϡˮ��Һ������Ҫ�ɷ��� ![]() ��
�� ![]() ��
�� ![]() ��Ũ������ˮ���٣�����ֻ�в��ֵ��룬����Ȼ��������ӵ���ʽ���ڡ�
��Ũ������ˮ���٣�����ֻ�в��ֵ��룬����Ȼ��������ӵ���ʽ���ڡ�
����ϡ��������������� ![]() �����֣������������ԡ�Ũ���������������������У�6�۵���Ԫ�������֣���ǿ�����ԡ�ͬ������Ũϡ������ɵIJ�ͬ��Ũ������ֳ�ϡ������û�е���ˮ�ԡ���ˮ�ԡ�
�����֣������������ԡ�Ũ���������������������У�6�۵���Ԫ�������֣���ǿ�����ԡ�ͬ������Ũϡ������ɵIJ�ͬ��Ũ������ֳ�ϡ������û�е���ˮ�ԡ���ˮ�ԡ�
����Ũ�������������ָ��������У�6�۵���������ԣ������������ӵ������ԡ����Ũ�����ڷ�Ӧ���Ƿ����������Կ���6�۵���Ļ��ϼ��Ƿ͡�
����Ũ���������������ṩ�����ӵ����ʣ������������ˮ�������ܰѷ�Ӧ������ˮ������ΪŨ�����Ƿ�������Ե�Ψһ��־��
![]()
![]()
![]()
�����÷�Ӧ�о�����ˮ���ɣ���Ũ������ֵ��������ԣ����������ԡ�����Ũ�����ڷ�Ӧ���������ṩ�����ӣ���Ȼ��
![]() ���ɡ�����������������
���ɡ�����������������
![]() ���������ж�Ũ�����Ƿ��ڷ�Ӧ�б������ԡ��磺
���������ж�Ũ�����Ƿ��ڷ�Ӧ�б������ԡ��磺
![]()
������Ӧ��Ũ����ȱ��������ֱ��������ԣ���������Ӧ��Ũ����ֻ���������ԡ�
![]()
![]()
![]()
ͭ��Ũ���ᷴӦʵ��ĸĽ�
�Ľ�ʵ�鷨һ
����һ��ʵ����Ʒ�� ��֧�ܵ��Թܡ�����̨�����С��ƾ��ơ��Թܡ�U�ιܡ��������ܡ���Ƥ����ֹˮ�кͽ�ͷ�ιܡ�
Ũ���ᡢϸͭ˿����ͭ˿��Ʒ����Һ��������ά��̿�ں���ʯ�ҡ�
��������ʵ�鲽��
����1�� ȡ�ʵ���С����Ƥ��һ������ճ��������ʿ�ֵĴָ�˿����Ƥ��ʹ֮������Ƥ���������ƶ����ڸ�˿���¶˰�������ϸͭ˿��
����2������������˿����U�ιܣ��ټ�����������ʯ�Һͻ���̿���������벣��˿���ٷ�����ʯ�Һͻ���̿����˷���ֱ��װ��U�ιܡ�ע��Ӧ����U�ι������ʵ����ɣ�����������ͨ��
����3�� ��ͼʾ���Ӻ�װ�ã������װ�õ������ԡ�
����4���ڸ��Թ��м�����ӦҩƷ�����Ӻ�װ�á�ʹֹˮ�д��ڿ���״̬��ע�ⲻҪ��ϸͭ˿����Ũ�����С�
����5������Ũ����������ʱ�����ָ�˿����Ũ�����У�ʹϸͭ˿��ȫ����Ũ���ᡣ���������Һ�ֹͣ���ȣ�����ϸͭ˿�����ᡣ����Ʒ����Һ������Ҫ�ر�ֹˮ�С�
����6��������ȴ���ý�ͷ�ι���ȥ�Թܼ��е��ϲ�Һ�塣���Թ��м���4��5����ˮ
��������ʵ������
������ʼʱ�Թܼ����д����İ������ɡ�������Ϊ����������ˮ��ϳ�������СҺ�ε�Ե�ʡ���˿�����ڣ����ŷ�Ӧ�ļ������У���ɫ������ʧ����Һ���ǣ�
���Թ���Ʒ����Һ����ɫ��ֹͣ���Ⱥ��Թܼĵײ��д�����ɫ�ľ��������������м�����������ˮ��
�����ġ��ĵ���
����1��ʱ��̣�Ч�ʸߡ� ���ڲ���ϸͭ˿����Ӧ�ٶȽϿ졣
ʱ��ֻ��2��3���ӡ� ϸͭ˿���Լ���ʹ�á������Ժ��������������ͭ��ʵ���б��ڹ۲졣
����2������Ⱦ����ʵ�������˷�����ߵ�ԭ������װ���н���U�ιܣ�
��װ����̿������˿����ʯ�ҡ�
����3����Ӧ��֣��������ԡ��뿴���¶Ա�ʵ�飺�ֱ�����ƿ����ʯ�������Ⱥ��Թ�ֱ�Ӽ��ȣ��������������ʯ�������ȵ�ʱ�䳤������Ӧ�����ĺ�ɫ����࣬���Թ��м��ȷ�Ӧʱ��̣���ɫ�����١��ɼ��������¶�Խ�ߣ�ʵ������Խ���ԡ�Ч��Խ�á���ʵ��������������Թ��м��ȣ���Ӧ��֣������˽϶�İ�ɫ����ͭ���壬�����ڸ������ɫ�����٣�
�����м�������ˮ�ɹ۲쵽��������ɫ��Һ���������ԡ�
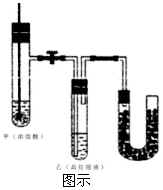
�Ľ�ʵ�鷨����
�������Թ��м���һ��ͭƬ��ע������Ũ���ᣬ����Ƭ�̡����Թܿڵ�ʪ�����ɫʯ����ֽ��죨SO2���ɣ���δ��Ӧ���ͭ�����ɫ�IJ�����Թܵײ����������ĻҺ�ɫ�ij��������Թ��ڵ���Һ������һ֧ʢ��ˮ���Թ��к��ѹ۲쵽��Һ��������ʵ�Ǻ�ɫ��������CuS��Cu2S������Һ�ɫ�ij�����CuS��Cu2S����CuSO4�Ļ���������Ӧ���ڷ�ˮ��Һ�н��еģ���Ӧ���������ɵ�������ˮ��ˮ�����ͷų������ɵ�CuSO4����û��ˮ�ܽ����ɫ���������Թ��С���Ӧ���Թ��е���Һ��������ŨH2SO4
��������ϡ�͵���H2SO4
������CuSO4��Һ���ʺ��ѹ۲쵽��Һ������Ϊ�������Եع۲쵽ʵ����������ʵ���в�ʹ֮������ɫ���ʣ�����ʵ������СС�ĸĶ�������������������£�
����1����1��Ԥ�Ƚ�һƬʪ�����ɫʯ����ֽ���ڲ������ϱ��ã�
������2����һ��ͭ�Ƶĵ��߰�ȥ���ϰ�Ƥ��¶��ͭ˿��Լ7��8���ף���ȡһ֧�ιܣ���ȥ��ͷ����������ιܣ�ʹͭ˿�ڼ����һ��¶����
����2�� �� һ֧�Թ��м�������ŨH2SO4
���̶�������̨�ϣ��þƾ��Ƽ������ӽ����ڡ�
����3�� ʵ��ʱ�ֳֵιܣ�ʹͭ˿¶����һ�����Ԥ�ȼ��ȵ�Ũ�����У�ͬʱ��������ֽ�IJ����������Թܿڡ���ʪ���ʯ����ֽ���ʱȡ��ͭ˿������Ƭ�̣����Թܵײ����Թ۲쵽�а�ɫ����������ˮCuSO4�����ɡ���ȴ�������ϲ�Һ�壬���Թ��м�������ˮ����ɫ�����ܽ�õ���ɫ��Һ��Ч�����á�
ץס���Խ���Ũ��������
����Ũ��������ɫ��״Һ�壬�ܶ� ![]() ���е�388�棬��һ�ѻӷ��Ե�ǿ�ᡣ����Ũ������ѻӷ��ԣ�����ȡ����������
���е�388�棬��һ�ѻӷ��Ե�ǿ�ᡣ����Ũ������ѻӷ��ԣ�����ȡ����������
![]()
![]()
![]()
![]()
![]()
![]()
Ũ���������һ�����ͨ���⣬�������������ԣ�
������1����ˮ�� Ũ����������ʪ��ˮ�������е�ˮ�֣��dz��õ���������
![]()
![]()
![]()
������2����ˮ�� Ũ�����ܰ��л�������е� ![]() ��
�� ![]() ��
�� ![]() ����ʽ��ȥ�����磺
����ʽ��ȥ�����磺
![]()
������ˮ������ˮ�����ű��ʲ��죬���ڻ�ѧ�仯��
������3�������� �������������Ԫ��Ϊ��6�ۣ�����������̬��������ԭ��ʱ����6�۵���ɻ�ԭΪ��4�۵���
![]() �����ֳ�Ũ�����ǿ�����ԡ����磺
�����ֳ�Ũ�����ǿ�����ԡ����磺
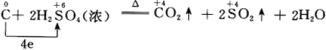
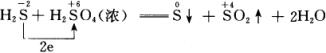
���磺
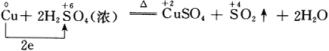
![]()
![]()
![]()
������Ũ����������ķ�Ӧ�У���Ϊ��������������ӵõ�2�����ӣ���ԭΪ����������ӣ������ɽ��������������õ����ᣬ��Ԫ�صĻ��ϼ��ڷ�Ӧǰ��û�з����仯�����ֳ���������ԡ��ӻ�ѧ����ʽ���Կ�������Ϊ���������õ���������Ϊ����õ���������ʵ�����������������ѧ��Ӧ��ǡ����ȡ�