 设为首页
设为首页
 加入收藏
加入收藏
例1 下表是元素周期表的一部分,回答下列有关问题:
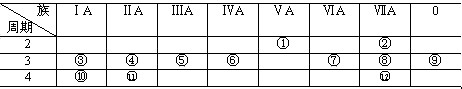
(1)写出下列元素符号:①
,⑥
,⑦
, ![]() 。
。
(2)在这些元素中,最活泼的金属元素是 ,最活泼的非金属元素是 ,最不活泼的元素是 。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 ,写出三者之间相互反应的化学方程式。
(4)在这些元素中,原子半径最小的是 ,原子半径最大的是 。
(5)在③与④中,化学性质较活泼的是 ,怎样用化学实验证明?答: 。在⑧与 12 中,化学性质较活泼的是 ,怎样用化学实验证明?答: 。
解析:解答本题关键要掌握:①1~20号元素的名称及符号;②元素周期表的结构;③能根据元素周期表中元素性质递变规律进行分析、判断。
答案:(1)N;Si;S;Ca (2)K;F;Ar
(3) ![]() ;
;
![]() ,
,
![]() ,
,
![]()
(4)K;F
(5)Na;可以用它们跟水反应的实验证明:钠跟水剧烈反应,放出氢气,并生成强碱;Mg跟沸水才反应,放出氢气,并生成中强碱
![]() ;
; ![]() ;可用氯气通入溴化钠溶液的实验证明:溶液呈棕红色,发生的反应为
;可用氯气通入溴化钠溶液的实验证明:溶液呈棕红色,发生的反应为 ![]() 。
。
例2 在下列各元素组中,除一种元素外,其余都可以按照某种共性归属一类,请选出各组的例外元素,并将该组其他元素的可能归属按所给六种类型的编号填入表内。
|
元素组 |
例外元素 |
其他元素所属编号 |
|
(1)S、Na、Mg |
||
|
(2)N、P、Sn、As |
||
|
(3)K、Ca、Al、Zn |
||
|
(4)Cu、Fe、Ag、Ca |
其他元素所属类型编号:①主族元素,②过渡元素,③同周期元素,④同主族元素,⑤金属元素,⑥非金属元素。
选题目的:此题考查学生对于周期表的结构是否熟悉。
解析:(1)中Na、Mg、S为同周期元素,(2)中N、P、As为ⅤA族元素,(3)中K、Ca、Al是主族元素,(4)中Cu、Fe、Ag是过渡元素
答案:(1)N,③(2)Sn,④(3) Zn,①(4) Ca,②。
例3 9.6g元素A与4.2g元素B含有相同的原子数,A和B原子核中质子数与中子数相等,已知A元素在其最高价氧化物中的含量是40%,在其氢化物中含量为94.1%。试计算A、B两元素的原子量,并推算出它们在周期表中的位置。
选题目的:此题通过计算推断元素在周期表中的位置,属于一道比较综合的练习题。
解析:
思路:(1)推出A的氢化物分子式为HxA,最高价氧化物分子式应该是A2O8-x,通过题给的条件求出A的原子量,(2)再利用题目中A、B质量关系和原子个数关系求出B的原子量,根据两种元素原子的质子数确定在周期表中的位置。
解:设该氢化物为:HxA,该最高价氧化物分子式应该为:A2O8-x
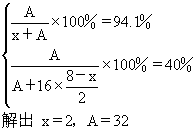
由于9.6g元素A与4.2g元素B含有相同的原子数,设B的原子量为y
由 ![]()
A的相对原子质量是32,其中子数与质子数相等,因此质子数为16的是硫元素,在第三周期ⅥA族。
B的相对原子质量是14,其中子数与质子数相等,因此质子数为7的是氮元素,在第二周期ⅤA族。
启示:此题最容易出错的是高价氧化物的分子式写不对,应由HxA推出A元素的最低价是-x,最高正价是8-x,从而得出氧化物的化学式为:A2O8-x。
例4 下列说法正确的是( )
(A)同一元素各核素的质量数不同,但它们的化学性质几乎完全相同
(B)任何元素的原子都是由核外电子和核内中子、质子组成的
(C)钠原子失去一个电子后,它的电子数与氖原子相同,所以变成氖原子
(D) ![]() 、
、 ![]() 、
、 ![]() 的质量数相同,所以它们是互为同位素
的质量数相同,所以它们是互为同位素
选题目的:本题是利用相关概念来对选项作出判断。
解析:对于A选项,可利用“结构决定性质”这一概念来进行判断;对于B选项,可利用部分原子结构的特殊性来解决;C选项中,必须明确决定原子种类的微粒是哪几种;D选项可用同位素的概念来进行判断。
A选项中的各核素是属同一元素,这些核素间必定互为同位素。根据同位素和质量数的含义可知:各核素原子的质子数同中子数不同,二者之和在数值上等于质量数,因而质量数必不相等,但同位素的化学性质几乎完全相同,故A选项正确。B选项中描述的只是原子构成的一般规律,而忽视了氕原子(
![]() )的原子核内只有质子而无中子这个特例,故B选项错误。C选项中原子种类应由质子数和中子数共同决定的,若原子核不改变,仅核外发生电子得失,是决不会发生由一种原子转变为另一种原子的,而只能由原子变为离子,故C选项错误。D选项中互为同位素的不同原子质子数相同,中子数不同,因而其质量数必然不等,故D选项错误。本题答案为A选项。
)的原子核内只有质子而无中子这个特例,故B选项错误。C选项中原子种类应由质子数和中子数共同决定的,若原子核不改变,仅核外发生电子得失,是决不会发生由一种原子转变为另一种原子的,而只能由原子变为离子,故C选项错误。D选项中互为同位素的不同原子质子数相同,中子数不同,因而其质量数必然不等,故D选项错误。本题答案为A选项。
答案:A
启示:此题的解题关键是要深刻理解有关同位素概念的内涵和外延,若概念模糊混淆,则易出现差错。
例5 X和Y是短周期元素,两者能组成化合物
![]() ,已知X的原子序数为n,则Y的原子序数不可能是 (
)
,已知X的原子序数为n,则Y的原子序数不可能是 (
)
A. ![]() B.
B.
![]() C.
C.
![]() D.
D.
![]()
选题目的:本题考查元素周期表的结构。
解析:由分子式 ![]() 可知X为+3价,Y为-2价,且X为最高正价,则为ⅢA族元素,Y为ⅥA族元素。
可知X为+3价,Y为-2价,且X为最高正价,则为ⅢA族元素,Y为ⅥA族元素。
(1)X、Y为同周期元素:
①均为第二周期元素,X(+3)为B,原子序数为5,则Y为氧元素其原子序数为5+3=8(C选项)。
②均为第三周期,X为Al,原子序数为13,则Y为硫元素,其原子序数为13+3=16(C选项)。
(2)X、Y不同周期:
①X在第二周期,Y在第三周期。
X为B,原子序数为5,则Y为硫,原子序数为 5+11=16(A选项)。
②X在第三周期,Y在第二周期。
X为Al,原子序数为13,则Y为氧,原子序数为 13-5=8(B选项)。
根据以上推算,Y的原子序数为 ![]() 的不可能存在。
的不可能存在。