 ЩшЮЊЪзвГ
ЩшЮЊЪзвГ
 МгШыЪеВи
МгШыЪеВи
ЁЁЁЁР§1 ТШЛЏфхЪЧгЩСНжжТБЫиЛЅЯрЛЏКЯЖјГЩЕФТБЫиЛЅЛЏЮяЃЌЦфЛЏбЇаджЪгыCl2ЯрЫЦЃЌФмгыН№ЪєКЭЗЧН№ЪєЗДгІЩњГЩТБЛЏЮяЃЌвВФмгыЫЎЗДгІЃКBrCl ЃЋ H2OЃНHClЃЋ HBrOЃЌЯТСагаЙиBrClЕФаджЪЕФа№ЪіжаВЛе§ШЗЕФЪЧЃЈ ЃЉ
ЁЁЁЁA. ЪЧНЯЧПЕФбѕЛЏМС
ЁЁЁЁB. ЗаЕуНщгкBr2гыCl2жЎМф
ЁЁЁЁC. ФмЪЙЪЊШѓЕФЕэЗлЕтЛЏМиЪджНБфРЖ
ЁЁЁЁD. BrClгыЫЎЗДгІжаЃЌBrClМШЪЧбѕЛЏМСгжЪЧЛЙдМС
ЁЁЁЁбЁЬтФПЕФЃКBrClбЇЩњВЛЪьЯЄЃЌДЫЬтЪєгкаХЯЂЬтЃЌЬтжаЬсЪОЦфаджЪгыТШЦјЯрЫЦЃЌШчКЮРћгУЫљИјаХЯЂНтЬтЪЧбЕСЗЕФжиЕуЁЃДЫЬтВЛФбЃЌЕЋЪЧГіДэТЪКмИпЁЃ
ЁЁЁЁНтЮіЃКBrClЕФаджЪгІИУНщгкCl2ЁЋBr2жЎМфЃЌОпгаНЯЧПЕФбѕЛЏадЃЌBrClЕФЪНСПНщгкCl2ЁЋBr2жЎМфЃЌЗжзгМфзїгУСІвВНщгкCl2ЁЋBr2жЎМфЃЌвђДЫЗаЕугІНщгкCl2ЁЋBr2жЎМфЁЃгЩгкфхЕФЗЧН№ЪєадБШТШЕФШѕЃЌПЩжЊдкBrClжаBrЮЊЃЋ1МлЃЌClЮЊЃ1МлЃЌгыЫЎЗДгІЪБЛЏКЯМлУЛгаБфЛЏЃЌЪєгкЗЧбѕЛЏЛЙдЗДгІЃЌЙЪBrClМШВЛЪЧбѕЛЏМСвВВЛЪЧЛЙдМСЁЃBrClПЩвдКЭKIЗДгІЩњГЩЕтЕЅжЪЃЌгіЕэЗлБфРЖЁЃBrClЃЋ2KI ЃН I2 ЃЋ KClЃЋ KBr
ЁЁЁЁД№АИЃКD
ЁЁЁЁЦєЪОЃКДЫЬтжаBrClбЇЩњВЛЪьЯЄЃЌЕЋЪЧТШЦјЕФаджЪКЭТБЫиЕФгаЙиаджЪЕФЕнБфЙцТЩЪЧЧхГўЕФЃЌгІгУЙцТЩжИЕМНтЬтЪЧбЇЩњбЇЯАЙ§ГЬжаБШНЯРЇФбЃЌЛђепЫЕдЫгУФмСІБШНЯВюЕФЗНУцЃЌНЬЪІгІзЂвтетРрЪдЬтЕФбЕСЗЁЃ
ЁЁЁЁР§2 МзЁЂввЁЂБћШ§жжШмвКИїКЌгавЛжж
![]() ЃЈ
ЃЈ ![]() ЮЊ
ЮЊ ![]() ЁЂ
ЁЂ ![]() Лђ
Лђ ![]() ЃЉРызгЃЌМзжаМгЕэЗлШмвККЭТШЫЎЃЌдђШмвКБфЮЊГШЩЋЃЌдйМгБћШмвКЃЌШмвКЮоУїЯдБфЛЏЃЌдђМзЁЂввЁЂБћвРДЮЮЊЃЈ
ЃЉ
ЃЉРызгЃЌМзжаМгЕэЗлШмвККЭТШЫЎЃЌдђШмвКБфЮЊГШЩЋЃЌдйМгБћШмвКЃЌШмвКЮоУїЯдБфЛЏЃЌдђМзЁЂввЁЂБћвРДЮЮЊЃЈ
ЃЉ
ЁЁЁЁAЃЎ
![]() ЁЁЁЁBЃЎ
ЁЁЁЁBЃЎ
![]()
ЁЁЁЁCЃЎ
![]() ЁЁЁЁDЃЎ
ЁЁЁЁDЃЎ
![]()
ЁЁЁЁЗжЮіЃКИљОнТБЫидзгЗЧН№ЪєадАДFЁЂClЁЂBrЁЂIЫГађж№НЅМѕШѕЃЌТБЫиРызгАД
![]() ЛЙдадж№НЅдіЧПЕФЕнБфЙцТЩЗжЮіЃК
ЛЙдадж№НЅдіЧПЕФЕнБфЙцТЩЗжЮіЃК
ЁЁЁЁМзШмвКМгЕэЗлКЭТШЫЎКѓЃЌЮДГіЯжРЖЩЋЃЌЕэЗлгіЕтБфРЖЩЋЃЌЫЕУїМзШмвКжаВЛКЌга
![]() ЁЃЖјШмвКГЪГШЩЋЃЌМДЮЊфхЫЎЕФбеЩЋЃЌЫЕУїМзШмвККЌга
ЁЃЖјШмвКГЪГШЩЋЃЌМДЮЊфхЫЎЕФбеЩЋЃЌЫЕУїМзШмвККЌга
![]() ЁЃдйМгБћШмвКЃЌШєБћШмвКжаКЌга
ЁЃдйМгБћШмвКЃЌШєБћШмвКжаКЌга ![]() ЃЌдђЛсга
ЃЌдђЛсга ![]() ЩњГЩЖјгіЕэЗлБфРЖЩЋЃЌЕЋУЛгаДЫЯжЯѓГіЯжЃЌЫЕУїБћШмвКжаЮо
ЩњГЩЖјгіЕэЗлБфРЖЩЋЃЌЕЋУЛгаДЫЯжЯѓГіЯжЃЌЫЕУїБћШмвКжаЮо
![]() РызгЖјКЌга
РызгЖјКЌга ![]() ЃЌдђввШмвКжаКЌга
ЃЌдђввШмвКжаКЌга ![]() ЁЃ
ЁЃ
ЁЁЁЁД№АИЃКBбЁЯюЗћКЯЬтвтЁЃ
ЁЁЁЁЦєЪОЃКЖдТБЫиМфжУЛЛЕФЙцТЩВЛЧхГўЛђТБЫиЕЅжЪбеЩЋВЛУїШЗЃЌОЭЛсдьГЩДэЮѓЃЌжЛгаеЦЮеЛљДЁжЊЪЖЃЌВХФмЬсИпФмСІЁЃ
ЁЁЁЁР§3 эСЃЈAtЃЉЪЧдзгађЪ§зюДѓЕФТБзхдЊЫиЃЌЭЦВтэСЛђэСЕФЛЏКЯЮязюВЛПЩФмОпгаЕФаджЪЪЧЃЈ ЃЉ
ЁЁЁЁAЃЎ ![]() КмЮШЖЈЁЁЁЁЁЁЁЁBЃЎэСвзШмгкгаЛњШмМС
КмЮШЖЈЁЁЁЁЁЁЁЁBЃЎэСвзШмгкгаЛњШмМС
ЁЁЁЁCЃЎ ![]() ВЛШмгкЫЎЁЁЁЁDЃЎэСЪЧгаЩЋЙЬЬх
ВЛШмгкЫЎЁЁЁЁDЃЎэСЪЧгаЩЋЙЬЬх
ЁЁЁЁЗжЮіЃКдкжабЇЛЏбЇПЮБОжаЃЌОЁЙмУЛгаНщЩмЙ§эСКЭэСЕФЛЏКЯЮяЕФаджЪЃЌЕЋдЫгУТБЫиаджЪЕФЕнБфЙцТЩЃЌПЩвдЭЦЖЯГіэСКЭэСЕФЛЏКЯЮяПЩФмОпгаЛђВЛПЩФмОпгаЕФаджЪЁЃР§ШчТШЪЧЛЦТЬЩЋЦјЬхЁЂфхЪЧзиКьЩЋвКЬхЁЂЕтЪЧзЯКкЩЋЙЬЬхЃЌПЩвдЭЦВтэСвВПЩФмЪЧгаЩЋЙЬЬхЃЛИљОн
![]() ЁЂ
ЁЂ ![]() ЁЂ
ЁЂ ![]() ЖМВЛШмгкЫЎЃЌПЩвдЭЦЖЯ
ЖМВЛШмгкЫЎЃЌПЩвдЭЦЖЯ ![]() вВПЩФмВЛШмгкЫЎЃЛИљОнфхКЭЕтЖМвзШмгкФГаЉгаЛњШмМСЃЌПЩвдЭЦЖЯэСвВПЩФмШмгкФГаЉгаЛњШмМСЁЃЩЯЪіЫФЬѕЭЦТлгыБИбЁЯюDЁЂCЁЂBФкШнвЛжТЃЌЕЋТБЫиЧтЛЏЮяЕФЮШЖЈадЪЧ
вВПЩФмВЛШмгкЫЎЃЛИљОнфхКЭЕтЖМвзШмгкФГаЉгаЛњШмМСЃЌПЩвдЭЦЖЯэСвВПЩФмШмгкФГаЉгаЛњШмМСЁЃЩЯЪіЫФЬѕЭЦТлгыБИбЁЯюDЁЂCЁЂBФкШнвЛжТЃЌЕЋТБЫиЧтЛЏЮяЕФЮШЖЈадЪЧ
![]() ЃЌПЩвдЭЦЖЯЃЌ
ЃЌПЩвдЭЦЖЯЃЌ ![]() ПЩФмВЛКмЮШЖЈЃЌетгыбЁЯюВЛвЛжТЁЃ
ПЩФмВЛКмЮШЖЈЃЌетгыбЁЯюВЛвЛжТЁЃ
ЁЁЁЁД№АИЃКAбЁЯюЗћКЯЬтвтЁЃ
ЁЁЁЁЦєЪОЃКДЫЬтПМВщФмЗёСщЛюдЫгУТБзхдЊЫиаджЪЕФЕнБфЙцТЩЁЃ
ЁЁЁЁР§4 АДЯТЪіЪЕбщЙ§ГЬЬюПеЃК
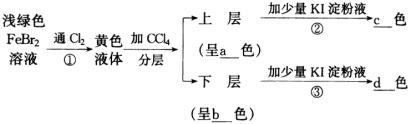
аДГіЩЯЪіЗДгІЕФЛЏбЇЗНГЬЪНЃК
ЁЁЁЁЂй ЃЛ
ЁЁЁЁЂк ЃЛ
ЁЁЁЁЂл ЃЛ
ЁЁЁЁЂм ЃЛ
ЁЁЁЁбЁЬтФПЕФЃКДЫЬтБШНЯзлКЯЕФПМВщСЫТБЫивЛНкЕФЪЕбщЁЃвЊЧѓбЇЩњФмЙЛзМШЗУшЪіЪЕбщЯжЯѓЃЌе§ШЗЪщаДЛЏбЇЗНГЬЪНЁЃДЫЬтжаТШЛЏЬњгыЕтЛЏМиЕФЗДгІгавЛЖЈФбЖШЃЌНЬЪІПЩвдЪЪЕБИјвдЬсЪОЁЃ
ЁЁЁЁНтЮіЃКвђЮЊЗЂЩњЗДгІЂйЃК
![]() ЃЌЫљвдМг
ЃЌЫљвдМг ![]() ЗжВуКѓЃЌЩЯВуЪЧ
ЗжВуКѓЃЌЩЯВуЪЧ ![]() ЫЎШмвКЃЌГЪзиЛЦЩЋЃЈaДІЃЉЃЌЯТВуЪЧШмгафхЕФ
ЫЎШмвКЃЌГЪзиЛЦЩЋЃЈaДІЃЉЃЌЯТВуЪЧШмгафхЕФ ![]() ЃЈгЭВуЃЉЃЌГЪГШКьЩЋЃЈbДІЃЉЁЃдкЩЯВу
ЃЈгЭВуЃЉЃЌГЪГШКьЩЋЃЈbДІЃЉЁЃдкЩЯВу ![]() ШмвКжаМгШыKIЕэЗлвКЃЌвђЮЊ
ШмвКжаМгШыKIЕэЗлвКЃЌвђЮЊ ![]() габѕЛЏадЃЌ
габѕЛЏадЃЌ ![]() гаЛЙдадЃЌЙЪЗЂЩњЗДгІЂкЃК
гаЛЙдадЃЌЙЪЗЂЩњЗДгІЂкЃК
![]() ЃЌ
ЃЌ ![]() ЪЙЕэЗлБфРЖЩЋЃЈcДІЃЉЁЃЯТВуМгШыKIЕэЗлвКЃЌвђЗЂЩњЗДгІЂлЃК
ЪЙЕэЗлБфРЖЩЋЃЈcДІЃЉЁЃЯТВуМгШыKIЕэЗлвКЃЌвђЗЂЩњЗДгІЂлЃК
![]() ЃЌЫфШЛДЫЗДгІвВЩњГЩСЫ
ЃЌЫфШЛДЫЗДгІвВЩњГЩСЫ ![]() ЃЌгыЩЯВуВЛЭЌЕФЪЧЕтгіЕэЗлВЂВЛЯдРЖЩЋЃЌЖјЪЧЕтДгЕэЗлШмвКжаБЛнЭШЁЕН
ЃЌгыЩЯВуВЛЭЌЕФЪЧЕтгіЕэЗлВЂВЛЯдРЖЩЋЃЌЖјЪЧЕтДгЕэЗлШмвКжаБЛнЭШЁЕН
![]() РяЃЌЕтдк
РяЃЌЕтдк ![]() РяЯдзЯЩЋЃЈdДІЃЉЁЃ
РяЯдзЯЩЋЃЈdДІЃЉЁЃ
ЁЁЁЁЦєЪОЃКфхКЭЕтдкЫЎжаШмНтадОљКмаЁЃЌЖјдкФГаЉгаЛњШмМСжаЃЈШчЃКБНЁЂЦћгЭЁЂЫФТШЛЏЬМЃЉдђвзШмЁЃЯТБэСаГіЕЅжЪфхЁЂЕтдкВЛЭЌШмМСжаЕФЯдЩЋЧщПіЁЃ
|
ЕЅжЪ |
ЫЎ |
БН |
ЦћгЭЁЂЫФТШЛЏЬМ |
|
фх |
ГШКь |
ГШКь |
ГШКь |
|
Ет |
ГШЛЦ |
зЯКь |
зЯКь |