 设为首页
设为首页
 加入收藏
加入收藏
例1 判断下列叙述正确的是
A.标准状况下,1mol任何物质的体积都约为22.4L
B.1mol任何气体所含分子数都相同,体积也都约为22.4L
C.在常温常压下金属从盐酸中置换出1molH2转移电子数为1.204×1024
D.在同温同压下,相同体积的任何气体单质所含原子数目相同
选题目的:这是一道基础知识概念的理解题,涉及气体摩尔体积、化学反应及物质结构的初步知识。适合中等学生。
思路分析:根据标准状况下气体摩尔体积的定义,应注意:一是标准状况,二是指气体的体积而非固体或液体的体积,所以A、B两项均错;C项正确,物质的微粒数不受外界条件影响而变化;D项错,气体单质分子,可以是单原子分子如He,也可以是双原子分子如H2,还可以是多原子分子如O3,因此相同温度压强下相同体积的任何气体虽然分子数相同,但所含原子数不一定相同。
解答:C.
启示:抓住基础知识和基本概念,不仅可以轻松地进行解题,而且对概念的理解更加准确和深刻。
例2 两个体积相同的密闭容器一个盛有氯化氢,另一个盛有H2和Cl2的混合气体,在同温同压下,两个容器内的气体一定具有相同的
A.质量 B.密度 C.分子总数 D.原子总数
选题目的:a.阿伏加德罗定律的运用。b.考察学生对知识的掌握及灵活运用的程度,提高思维能力。适合中等以上的学生。
思路分析:同温同压下两个容器体积相同,则所含的分子数相同,又因HCl、H2、Cl2都是双原子分子,故原子总数也相同,质量、密度不一定相同。
解答:C.D
启示:在同温同压下,两个体积相同的容器,不论是一种气体,还是混合气体含有的分子总数相同。
例3 如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
选题目的: 深刻理解物质的量、摩尔质量、质量、气体摩尔体积和粒子数之间的关系,培养分析、思维的能力。
思路分析:该气体的分子数为b,则物质的量为 ![]() mol,
mol,
摩尔质量M= 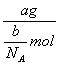 =
= ![]() g/mol,
g/mol,
cg气体的物质的量为
n= 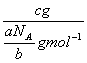 =
= ![]() mol.
mol.
cg该气体标况下体积V=n•22.4L/mol=
![]() mol×22.4L/mol=
mol×22.4L/mol= ![]() L
L
解答:D
启示:深刻理解概念,掌握解题思路。
例4 按体积比为4:2:3所组成的N2、O2、CO2,混合气体100g在标准状况下体积为___ L。
选题目的:a.学会求混合气体平均相对分子质量。b.加深对气体摩尔体积和阿伏加德罗定律的理解。
思路分析:先根据阿伏加德罗定律求出混合气体的平均相对分子质量,然后求出混合气体的物质的量,最后求出在标准状况下的体积。
根据阿伏加德罗定律,三种气体的体积比为4:2:3,物质的量之比也为4:2:3,可当作4mol,2mol,3mol.
![]() =
= ![]()
=34.2g/mol
混合气体总物质的量为
![]() =2.92mol
=2.92mol
体积应为 2.92 mol ×22.4 L/mol = 65.4 L
解答:65.4L
启示:阿伏加德罗定律的推论之一:同温同压下,任何气体的体积比等于它们的物质的量之比,即 ![]()