设为首页
设为首页
 加入收藏
加入收藏
典型例题
氧气的性质和用途
【例1】下列物质在氧气中燃烧时,集气瓶底部要垫少量细砂或水的是( )
A.木炭 B.硫粉 C.铁丝 D.红磷
分析:上述物质在氧气中燃烧时,只有选项(C)铁丝的集气瓶底部要垫少量的细砂或水。这是因为木炭、硫粉燃烧的产物是气体,红磷燃烧时冒白烟,说明产物是细小的白色颗粒,它们的逸散不会引起集气瓶底的炸裂。而铁丝在纯氧中燃烧时,火星四射,生成一种黑色的固体。由于燃烧时放出大量的热,使生成物熔化溅落下来,为了防止溅落的熔化物炸裂瓶底,所以瓶里要预先装少量的细砂或水。
解答:选(C)。
【例2】下列物质燃烧时,一定有火焰产生的是( )
A.镁条 B.木炭 C.铁丝 D.硫粉
分析:可燃物在空气或纯氧中燃烧时,一定发光放热,但不一定都有火焰,只有可燃性的气体(或蒸气)点燃时才有火焰产生。上述四个选项中,镁条、木炭、铁丝等固体物质燃烧时,既不挥发又不能分解出可然性的气体,因此只发光而无火焰产生。硫粉虽为固体粉末,但点燃后逐渐熔化且不断形成硫的蒸气而燃烧,因此有火焰产生。
解答:选(D)。
【例3】下列物质在空气中燃烧时,能产生大量的烟的是( )
A.木炭 B.红磷 C.铁丝 D.硫粉
分析:烟和雾是日常生活中常见的现象,它们是一回事吗?不是,科学上把大量的细小团体微粒悬浮在空气中的现象叫做“烟”;把大量的液体小液滴悬浮在空气中的现象叫作“雾”。本题的四个选项中,只有红磷在空气中燃烧,生成大量的五氧化二磷白色固体粉末,逸散在空气中,产生浓厚的白烟。
解答:选(B)。
【例4】下列反应中,既属于氧化反应又属于化合反应的是( )
A.铁+氧气 ![]() 四氧化三铁
四氧化三铁
B.磷+氧气 ![]() 五氧化二磷
五氧化二磷
C.酒精+氧气 ![]() 二氧化碳+水
二氧化碳+水
D.蜡烛+氧气 ![]() 二氧化碳+水
二氧化碳+水
分析:化合反应和氧化反应是从两个不同的侧面描述反应类型的方法,二者之间没有必然的联系。判断某化学反应是不是化合反应,要着眼于生成物是否只有一种物质,只有一种物质生成的化学反应才是化合反应。判断某化学反应是不是氧化反应,要着眼于参加化学反应的物质有没有跟氧发生反应,有氧参加的反应一定是氧化反应。由此判断,本题四个选项中涉及的四个化学反应,从反应物来看,均有氧参加反应,故均为氧化反应;从生成物来看,只有(A)和(B)是生成一种新物质的反应,属于化合反应,因此,既属于氧化反应又属于化合反应的化学变化是(A)和(B)。
解答:选(A)和(B)。
【例5】列表比较木炭、硫粉、红磷、铁丝、蜡烛在空气和氧气中燃烧的现象。
分析:对氧气化学性质的感性认识必须通过观察实验来完成。通过实验分析现象,得出结论,才能深刻地认识到:氧气是一种化学性质比较活泼的气体,能跟许多物质发生氧化反应。在反应中,氧气提供氧,具有氧化性,它是一种常用的氧化剂。
解答:物质在空气和氧气中燃烧现象的比较
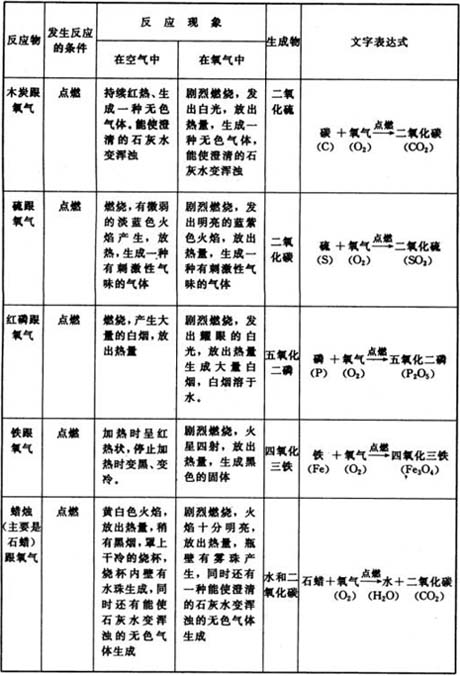
点拨:从上表的对比中,可以发现:
1.物质(当然是可以燃烧的物质)在空气中或氧气中要燃烧,需要一定的温度,一般都要进行点燃。
2.物质在纯氧中的反应比在空气中剧烈,在空气中不能燃烧的物质(如铁),在纯氧中却能燃烧起来,且十分剧烈。为什么呢?这是因为物质在空气中燃烧和在纯氧中燃烧的实质相同,都是跟氧气发生的化学反应,而空气中的氧气已经被近4/5体积的氮气所冲淡,所以反应现象不如在纯氧中剧烈。
3.不同物质燃烧时现象不同,同种物质在空气和氧气中燃烧时的现象也不尽相同,因此,要在观察的基础上有意记忆一些有特征的现象,以便进行物质的识别。
4.通过对比,加深对化合反应和氧化反应概念的理解,并能正确加以区分。
5.根据事实,能正确书写化学反应的文字表达式,并尽可能的记忆某些常见物质的化学符号,为以后学习铺垫好基础。
氧气的制法
【例1】氯酸钾分解制取氧气的必要条件是( )
A.加入少量二氧化锰 B.隔绝空气
C.加入少量高锰酸钾 D.加热到较高温度
分析:氯酸钾在较高温度(400℃以上)下,分解放出氧气,这是氯酸钾具有的化学性质,加热至较高温度(400℃以上)是氯酸钾分解放氧的必要条件。若不加热,在氯酸钾中加入二氧化锰或高锰酸钾,不论多与少都不会使氯酸钾分解放氧。隔绝空气跟氯酸钾能否分解毫无关系。故氯酸钾分解制氧的必要条件是加热至较高温度。
解答:选(D)。
【例2】二氧化锰可以加快任何化学反应的反应速率,因为它是催化剂。这句话正确吗?为什么?
分析:这种说法不正确。造成错误的原因是对催化剂概念理解不全面造成的。催化剂是指:在化学中能改变其他物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有变化的物质。该定义中的“改变”包含加快或减慢反应速率两种可能。工业上把使化学反应速率加快的催化剂,叫做正催化剂;使化学反应速率减慢的催化剂,叫做负催化剂,所以不能把“改变”其他物质的反应速率,片面地理解为“加快”反应速率。另外,催化剂一般具有选择性,它只能改变某个反应或某一类反应的反应速率。例如,二氧化锰对氯酸钾受热分解起催化作用,但对高锰酸钾的受热分解不起催化作用,而是高锰酸钾分解后的一种生成物。因此,认为二氧化锰能改变任何化学反应的反应速率的说法是错误的。正确的说法是:在氯酸钾受热分解的反应中,可选择二氧化锰作催化剂,二氧化锰可使氯酸钾在较低温度下迅速放出氧气。
解答:同上。
【例3】下列气体中,既能用排水取气法又能用向上排空气法收集的气体是( )
|
A.氧气 |
B.氢气 |
C.二氧化碳 |
D.甲烷 |
|
|
标准状况下密度 |
1.429克/升 |
0.089克/升 |
1.978克/升 |
0.714克/升 |
|
在水中的溶解性 |
不易溶于水 |
难溶于水 |
能溶于水 |
难溶于水 |
(在标准状况下,空气的密度是1.293克/升)
分析:气体的收集方法是由该气体的物理性质决定的。难溶于水或不易溶于水的气体,可以用排水取气法收集;在相同条件下,密度比空气大的气体,可用向上排空气集气法收集;密度比空气小的气体,可用向下排空气集气法收集。为了将集气瓶内的空气排除干净,收集到较纯净的气体,排气集气时都应当把导管伸入集气瓶的底部。
上述四种气体中,既能用排水取气法收集又能用向上排空气法收集的气体是氧气。
解答:选(A)。
【例4】给固体药品加热时,为什么试管口一般要稍向下倾斜?
分析:给固体药品加热,一般选用试管,加热时,试管口要稍向下倾斜。原因是固体药品表面往往含有极少量的水分,加热时这些水分变为水蒸气蒸发,在试管口遇冷,部分水蒸气冷凝成水;有的固体药品受热时,能生成水,为了防止冷凝的水蒸气或反应后生成的水流到热的试管底部引起试管的破裂,所以给固体药品加热时,试管口一般要稍向下倾斜。
解答:同上。
【例5】化合反应与分解反应的比较
分析:化合反应与分解反应均属于化学反应中的基本反应类型。对二者概念的理解可从感性到理性,从实例出发,进行比较,理解起来并不困难。下面列表将这两类反应进行一下比较。