 设为首页
设为首页
 加入收藏
加入收藏
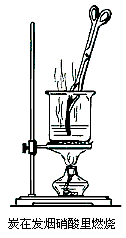
炭在发烟硝酸里燃烧
炭在浓硝酸里燃烧的实验
把一块红热的木炭(或用带火星的细木条)浸入热的发烟硝酸里,木炭燃烧得更加剧烈(或细木条着火燃烧),同时放出红棕色的二氧化氮气体,实验装置见下图:
硝酸合成与第一次世界大战
硝酸不仅是工农业生产的重要化工原料,而且也是制造炸药的重要战争物资。
当初制造硝酸 的方法是普通硝石法,即是硝石与硫酸反应,来制取硝酸的。但是硝石的贮量有限,因此硝酸的产量刀受到限制。
早在1913年之前,人们发现德国有屐世界大战的可能,便开始限制德国进口硝石。这样理以为世界会太平无事了。1914年德国终于发动了第一次世界大战,人们又错误地估计,战争顶多只会打半年,原因是德国的硝酸不足,火药生产受到了限制,由于人们的种种错误分析,使得第一次世界大战蔓延开来,战争打了四个多年头,造成了极大的灾难,夺去了人们无数的生命财产。德国为什么能坚持这么久的战争呢?是什么力量在支持着它呢?这就是化学,德国人早就对合成硝酸进行了研究。
1908年,德国化学家哈柏首先在实验室用氢和氮气在600℃200大气压下合成了氨,产率虽只有2%,这也是一项重大的突破。后由布什提高了产率,完成了工业化设计、建立了年产1000吨氨的生产装置、用氨氧化法可生产3000吨,硝酸,利用这些硝酸可制造3500吨烈性炸药TNT。这项工作已在大战前的1913年便完成了。这就揭开了第一次世界大战中的一个谜。
硝酸性质的实验
1.实验注意事项
(1)硝酸是强腐蚀性酸,应要求学生严格遵守使用强酸的有关规定,注意安全,防止硝酸溅到衣服或皮肤上。
(2)尽量防止氮的氧化物外逸,避免空气污染,影响师生健康。为此,硝酸的用量不宜过多,实验后,应将气体导管插入盛有石灰水或烧碱溶液的烧杯里。
2.有关稀硝酸跟铜反应的实验
(1)要把烧瓶里的空气排尽后再收集一氧化氮。反应一开始,烧瓶里往往出现红棕色,这是由于一氧化氮被烧瓶里的空气氧化的缘故。为此,一定要等产生的气体不带颜色或稍带红棕色时,方能开始收集一氧化氮。
(2)可以用大试管代替烧瓶作反应容器,以节约药品。
可提出下列问题,让学生进行思考、讨论。
(1)实验室应怎样保存浓硝酸?为什么?
(2)浓、稀硝酸都能跟铜片发生反应,而盐酸却不能,为什么?
(3)为什么一氧化氮可用排水集气法收集,不能用排空气集气法收集,而二氧化氮则相反?
(4)硝酸的氧化性表现在什么地方?