 ЙиОӘКЧТі
ЙиОӘКЧТі
 јУИлКХІШ
јУИлКХІШ
ҪМІД·ЦОцЈә
Ј Ј ұҫҪЪҪМІДУРТФПВБҪёцМШөгЈәЈЁ1Ј©¶ФУліхЦРЦӘК¶УРҪ»ІжөДДЪИЭЈ¬УРөДКЗІЙИЎЧЫәПБРұнөД·Ҫ·ЁЈ¬УРөДФтКЗІЙУГМЦВЫөД·Ҫ·ЁЈ¬ИГС§ЙъНЁ№эМЦВЫІўФЛУГіхЦРС§№эөДЦӘК¶Ј¬ҙУЦРЧЬҪбіц№жВЙРФЎЈЈЁ2Ј©ФӘЛШЦЬЖЪВЙөДөјіцТФАнВЫОӘЦёөјЈ¬ТФКВКөОӘТАҫЭЎЈҫЙҪМІДЦРөДФӘЛШЦЬЖЪВЙЦӘК¶Ј¬НкИ«КЗАнВЫөДНЖөјЎЈРВҪМІДЦРөДФӘЛШЦЬЖЪВЙЦӘК¶өДөГіцЈ¬І»ҪцУРАнВЫНЖөјЈ¬»№НЁ№эұИҪПН¬ЦЬЖЪФӘЛШөДРФЦК¶ФАнВЫНЖөјҪшРРБЛСйЦӨЎЈ¶шЗТЈ¬АнВЫНЖөјТІҙУіВКцКҪёДОӘУЙС§ЙъЧФјәҪшРРМҪЛчөД·ҪКҪҪшРРЎЈЦБҙЛОӘЦ№С§ЙъТСҫӯС§П°БЛСхЎўЗвЎўМјЎўМъөИФӘЛШј°ЖдТ»Р©»ҜәПОпЈ¬»№С§П°БЛјоҪрКфЎўВұЛШБҪёцФӘЛШЧеөДЦӘК¶Ј¬іхІҪС§П°БЛФӯЧУҪб№№өДАнВЫЦӘК¶ЎЈФЪХвёц»щҙЎЙПЈ¬ТэөјС§ЙъМҪЛчФӘЛШРФЦКәНФӯЧУҪб№№өД№ШПөЈ¬ҪТКҫФӘЛШЦЬЖЪВЙөДКөЦКЈ¬КЗК®·ЦұШТӘөДЎЈОӘБЛФцЗҝЖф·ўРФЈ¬ҪМІДІ»КЗЦұҪУёшіцФӘЛШЦЬЖЪВЙЈ¬¶шКЗНЁ№эҝОМГМЦВЫәНұЯҪІұЯКөСйЈ¬ТэөјС§Йъ¶ФҙуБҝКэҫЭәНКВКөҪшРР·ЦОцЈ¬ЧЬҪб№йДЙіцЦЬЖЪВЙЎЈХвСщ¶ФУЪЕаСшС§ЙъөДВЯјӯНЖАнДЬБҰК®·ЦУРАыЎЈ
Ј Ј ұҫҪЪҪМС§ЦШөгЈәФӯЧУөДәЛНвөзЧУІгЕЕІјәНФӘЛШҪрКфРФЎў·ЗҪрКфРФұд»ҜөД№жВЙЎЈ
Ј Ј ұҫҪЪҪМС§ДСөгЈәФӘЛШҪрКфРФЎў·ЗҪрКфРФұд»ҜөД№жВЙЎЈ
ҙУ¶аёцІгҙОАнҪвФӘЛШЦЬЖЪВЙ
ЎЎЎЎФӘЛШЦЬЖЪВЙКЗСРҫҝФӘЛШјдөДПа»ҘБӘПөәНұд»Ҝ№жВЙЎЈЛьөДҫЯМеДЪИЭКЗЈәФӘЛШөДФӯЧУҪб№№әНРФЦКЛжЧЕФӯЧУРтКэөДөЭФц¶шіКПЦЦЬЖЪРФұд»ҜөД№жВЙЎЈ
ЎЎЎЎ¶ФУЪФӘЛШЦЬЖЪВЙЈ¬УҰҙУұҫЦКөДЎўёРРФөДЎўұзЦӨөДЎўІ»Н¬ІгҙОЎўІ»Н¬ҪЗ¶ИИҘАнҪвЎЈ
ЎЎЎЎҙУұҫЦКЙПҝҙЈ¬ФӘЛШЦЬЖЪВЙКЧПИКЗФӯЧУҪб№№өДЦЬЖЪРФұд»ҜЎЈҙУ1Ў«18әЕФӘЛШЈ¬ЛжЦКЧУКэөЭФцЧоНвІгөзЧУКэЎўФӯЧУ°лҫ¶¶јіКЦЬЖЪРФұд»ҜЎЈЧоНвІгөзЧУКэәНФӯЧУ°лҫ¶ЦұҪУУ°ПмЧЕФӘЛШөДРФЦКЈ¬ТтҙЛФӯЧУҪб№№өДЦЬЖЪРФұд»Ҝҫц¶ЁБЛФӘЛШРФЦКөДЦЬЖЪРФұд»ҜЎЈАэИзФӘЛШ»ҜәПјЫМШұрКЗЧоёЯХэјЫЛжЧЕЦКЧУКэөДөЭФцЈ¬¶шіКПЦ+1ЦБ+7өДұд»Ҝ№жВЙЎЈФӘЛШөДҪрКфРФЎў·ЗҪрКфРФТІЛжЧЕФӯЧУРтКэөДөЭФц¶шіКПЦ№жВЙРФұд»ҜЎЈХвМеПЦБЛҪб№№ҫц¶ЁРФЦКЎЈ
ЎЎЎЎҙУёРРФЙПАнҪвФӘЛШЦЬЖЪВЙЎЈФЪС§П°ФӘЛШЦЬЖЪВЙЦ®З°Ј¬ТСҫӯС§П°БЛВұЛШЎўјоҪрКф2ёцЦчЧеФӘЛШЧеЎЈҫЯұёБЛТ»¶ЁөДФӘЛШ»ҜәПОпЦӘК¶Ј¬ФЪАнҪвФӘЛШЦЬЖЪВЙКұЈ¬ТФХвР©ЦӘК¶ОӘІДБПЈ¬Ҫ«ТСС§ФӘЛШ»ҜәПОпЦӘК¶әНРВС§өД»щұҫАнВЫУР»ъөШҪбәПЖрАҙЈ¬јИДЬёьәГөШАнҪвАнВЫЈ¬УЦДЬҪшТ»ІҪИПК¶ФӘЛШ»ҜәПОпЎЈАэИзЈ¬ФӘЛШЦЬЖЪВЙЦёіцФӘЛШөДФӯЧУҪб№№ЛжЧЕФӯЧУРтКэөДөЭФц¶шіКПЦЦЬЖЪРФөДұд»ҜЎЈИзәОұд»ҜЈҝЗлҝҙИэЧеФӘЛШВұЛШҙУFөҪAtЈ¬ФӯЧУҪб№№ИзПВЈә
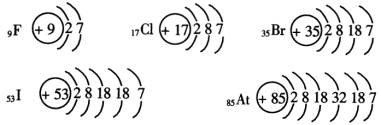
ЎЎЎЎЛжЧЕФӯЧУРтКэҙУ9өҪ85Ј¬ФӯЧУәЛНвөзЧУІгКэҙУ2ІгөҪ5ІгЈ¬іКөЭФцЗчКЖЈЁФӯЧУөД°лҫ¶ЦрҪҘФцҙуЈ©Ј¬ЧоНвІгөзЧУКэ¶јОӘ7ёцЎЈ
ЎЎЎЎЧчОӘҪрКфЧеөДҙъұнОпјоҪрКфЧеТІУРПаН¬өД№жВЙЎЈФӯЧУҪб№№ИзПВЈә
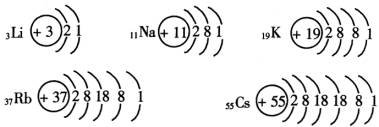
ЎЎЎЎҙУ3әЕLiөҪ55әЕCsЈ¬ЛжЧЕФӯЧУРтКэҙУ3өҪ55өЭФцЈ¬ФӯЧУәЛНвөзЧУІгКэөЭФцЈ¬ҙУ2ІгөҪ6ІгЎЈФӯЧУөД°лҫ¶ТІЦрҪҘФцјУЈ¬ЧоНвІгөзЧУКэ¶јПаН¬Ј¬КЗ1ёцөзЧУЎЈ
ЎЎЎЎУЙҙЛҝЙјыЈ¬УГ·бё»өДКөјКЦӘК¶ИҘАнҪвТ»ёцРВС§өДАнВЫ№жВЙЈ¬ұгУЪХЖОХХвТ»АнВЫЈ¬ҙУ¶шТІ№®№МБЛТСС§өДКөјКЦӘК¶ЎЈ
ЎЎЎЎТӘұзЦӨөШАнҪвФӘЛШЦЬЖЪВЙЎЈФӘЛШЦЬЖЪВЙЦёіцФӘЛШөДФӯЧУҪб№№әНРФЦК¶јЛжФӯЧУРтКэөДөЭФц¶шіКПЦЦЬЖЪРФұд»ҜЎЈЛщОҪЎ°ЦЬЖЪРФұд»ҜЎұИзәОАнҪвЈҝҪбәПЦЬЖЪұнАҙҝҙЈ¬ОЮВЫКЗН¬Т»ЦЬЖЪФӘЛШЈ¬»№КЗН¬Т»ЦчЧеФӘЛШЈ¬ФӯЧУөДәЛНвөзЧУЕЕІјЎўФӯЧУ°лҫ¶ЎўФӘЛШөД»ҜәПјЫЈ¬ТФј°ФӘЛШөДҪрКфРФЎў·ЗҪрКфРФ¶јіКПЦТ»¶ЁөДЦЬЖЪРФұд»ҜЎЈө«КЗЈ¬КВОп¶јУРБҪ·ҪГжЎЈФЪУҰУГФӘЛШЦЬЖЪВЙКұЈ¬јИТӘҝјВЗФӘЛШЧеөДНЁРФЈ¬УЦТӘҝјВЗөҪФӘЛШјдөДІоТмРФЈ¬І»ҝЙТ»О¶ХХ°бХХМЧЎЈХэПс»ҜС§ЦРіЈЛөөДТ»ҫд»°Ў°Ҫб№№ҫц¶ЁРФЦКЎұЎЈөұН¬ЧеФӘЛШөДФӯЧУҪб№№ПаН¬КұЈ¬ҫц¶ЁБЛФӘЛШРФЦКөДПаЛЖРФЈ»өұН¬ЧеФӘЛШөДФӯЧУҪб№№іцПЦІоТмРФКұЈ¬ФӘЛШөДРФЦКҫНіКПЦөЭұдРФЎЈФӘЛШЦЬЖЪВЙХэКЗЦёФӘЛШРФЦКөДПаЛЖРФәНөЭұдРФөДұзЦӨНіТ»ЎЈ