 设为首页
设为首页
 加入收藏
加入收藏
扩展资料
学法启示
1.化学方程式中,各物质的化学计量数(v)之比,等于各物质的物质的量(n)之比。即均等于该化学方程式的“系数”之比。
2.化学方程式中各气体在同温同压下的体积比,等于它们的化学计量数之比。即等于各气体在化学方程式中的“系数”比。
3.遇到有关化学方程式的计算时,经常视情况将相关物质的质量,一定浓度和体积的溶液、气体体积换算出它们的物质的量,按化学计量数找出比例关系后入手运算。
【知识要点】
1. 化学方程式中有关量的关系

由上可看出,化学方程式中各物质的化学计量数之比等于组成各物质的粒子数之比,等于各物质的物质的量之比,等于气体体积比(同状况下),不等于质量之比。根据化学方程式列比例时应遵循上述比例关系。
2.根据化学方程式计算时所列比例是否正确的判断依据是:“上、下单位要一致,左右单位要对应”。如:
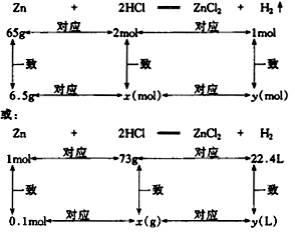
3.物质的量应用于化学方程式计算的一般格式
(1)设所求物质的物质的量为n(B)[或质量m(B)],或气体标准状况下体积V(B)、或溶液体积V[B(aq)]J。
(2)写出有关反应的化学方程式。
(3)在化学方程式有关物质的化学式下面先写出已知物和所求物的有关量的关系,再代入已知量和所求量。
(4)写出所求物质的数学表达式。
(5)写出解答和答案。
如:6.5g Zn在与足量盐酸反应时产生的
![]() 在标准状况下的体积是多少升?
在标准状况下的体积是多少升?
解:设产生 ![]() 的体积为V(
的体积为V( ![]() )
)
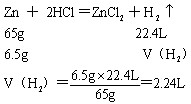
答:产生的 ![]() 在标准状况下的体积是2.24L。
在标准状况下的体积是2.24L。
4.规范用语
![]() ―表示
―表示 ![]() 的物质的量
的物质的量
![]() ―表示方程式中
―表示方程式中 ![]() 的化学计量数
的化学计量数
![]() ―表示盐酸的物质的量浓度
―表示盐酸的物质的量浓度
![]() ―表示
―表示 ![]() 溶液的体积
溶液的体积
![]() ―表示
―表示 ![]() 的体积
的体积
![]() ―表示混合物中
―表示混合物中 ![]() 的质量分数
的质量分数
![]() ―表示
―表示 ![]() 的质量
的质量
在列比例及运算过程中都应带单位。
扩展资料
化学计算的常用方法
一、平均值法
例1:由两种金属组成的合金5g与足量的氯气完全反应后增重7.1g,则该合金可能是( )
(A)Cu、Zn (B)Na、Al (C)Fe、Mg (D)Fe、Cu
解析:用平均值法解题比较简便。首先把5g合金看成一种金属,根据与氯气反应的质量求出其相对原子质量,为计算的方便,可以把金属定为二价金属,则有如下关系:
![]()
只有一种相对原子质量大于50的金属和一种相对原子质量小于50的金属按照一定比例组合成合金,其平均相对原子质量才能为50。由Cu、Zn组成的合金就不合题意。上述的计算是以二价金属为标准进行的。若不是二价金属可以按反应中消耗氯的量进行转换。以金属铝为例,71g氯气消耗金属铝18g,所以若把金属铝作为二价金属对待,则相对原子质量可取为18。同理,钠作为二价金属对待,相对原子质量可取为46。铁与氯气反应时为三价,若作为二价,相对原子质量可取为37.3。在转换后,才能根据组成平均相对原子质量为50的合金时,对各成分金属相对原子质量要求进行比较,只有D选项合理。
二、守恒法
例2:取钠、钙各一小块,投入适量水中,反应完毕时共收集氢气1.568L(标准状况)。再取碳酸钠和碳酸氢钠的混合粉末3.8g,溶于适量水中。将以上所得的两种溶液合并,恰好使溶液中 ![]() 、
、 ![]() 、
、 ![]() 等离子均进入沉淀。反应完毕后,将溶液蒸干得到8.8g白色固体,再将该白色固体洗涤干燥,得到白色不溶物4g。试求钠、钙各多少克?混合物中碳酸钠、碳酸氢钠的质量各多少克?
等离子均进入沉淀。反应完毕后,将溶液蒸干得到8.8g白色固体,再将该白色固体洗涤干燥,得到白色不溶物4g。试求钠、钙各多少克?混合物中碳酸钠、碳酸氢钠的质量各多少克?
解析:依题意,得到的8.8g白色固体为碳酸钙和氢氧化钠混合物,4g固体只为碳酸钙,其物质的量为: ![]() ,所以钙元素的质量=0.04×40=1.6g由钙产生的氢气为:0.04×22.4=0.896L,由钠产生的氢气为:1.568-0.896=0.672L。所以钠的质量为:
,所以钙元素的质量=0.04×40=1.6g由钙产生的氢气为:0.04×22.4=0.896L,由钠产生的氢气为:1.568-0.896=0.672L。所以钠的质量为: ![]()
设碳酸钠的物质的量为x,碳酸氢钠的物质的量为y
依据钠元素守恒,金属钠、碳酸钠与碳酸氢钠中钠原子的总物质的量等于8.8g固体中氢氧化钠的物质的量,可以列方程组:
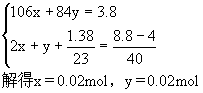
所以碳酸钠的质量:0.02×106=2.12g,碳酸氢钠的质量:0.02×84=1.68g
三、十字交叉法
例3:将金属钠在空气中燃烧,生成 ![]() 与
与 ![]() 的混合物。取该燃烧产物7.48g溶于水制成1000mL溶液,取出10mL用0.1mol/L的盐酸中和,用去盐酸20mL,由此可知该产物中
的混合物。取该燃烧产物7.48g溶于水制成1000mL溶液,取出10mL用0.1mol/L的盐酸中和,用去盐酸20mL,由此可知该产物中
![]() 的质量分数约为( )
的质量分数约为( )
(A)16.6% (B)20% (C)80% (D)78.4%
解析:由于 ![]() ,所以可看出
,所以可看出 ![]() 与
与 ![]() 混合物的总物质的量等于氢氧化钠物质的量的
混合物的总物质的量等于氢氧化钠物质的量的 ![]() ,又
,又 ![]() 则
则 ![]() 与
与 ![]() 的混合物的平均相对分子质量为:
的混合物的平均相对分子质量为: ![]()
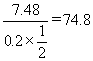 ,利用十字交叉求出二者物质的量之比
,利用十字交叉求出二者物质的量之比
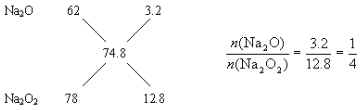
即混合物中 ![]() 的物质的量分数为20%,则其质量分数一定小于20%,故选A。
的物质的量分数为20%,则其质量分数一定小于20%,故选A。
四、差量法
例4:一块锌板的质量为13g,插到 ![]() 溶液中一段时间后取出,称其质量变为12.1g,求生成的铁是多少克?锌是否全部反应,若未完全反应,剩余锌多少克?
溶液中一段时间后取出,称其质量变为12.1g,求生成的铁是多少克?锌是否全部反应,若未完全反应,剩余锌多少克?

以上是化学计算中常用的方法,需要在不断的练习中总结、提高。