 设为首页
设为首页
 加入收藏
加入收藏
课题:铁的性质
重点:铁的化学性质
难点:对铁锈蚀条件及其防护措施的初步探究;对铁的化学性质比较活泼的理解。
课时安排:1课时
课前探究:
1. 查阅资料开展“铁的发现、存在和冶炼简史”、“铁的用途”的课题研究。并思考铁为什么会有这么多的用途。
2.查阅资料、社会调查等形式开展关于我国钢铁工业的发展的课题研究。
3.通过一组铁生锈的家庭实验:分析铁在什么条件下最容易生锈,及防止钢铁生锈的措施。(可以把书上的演示实验改进,如加热试管可改为在密闭容器中加入造量干燥剂。也可只做一个生锈的实验,并让学生思考“一个有一半浸在水中的铁钉,哪一部分锈斑最明显,为什么?)从而引导学生在以前研究灭火原理的基础上,运用相似的思维方法,总结分析出铁生锈的原理及防锈的方法。
4.通过观察、做社会调查等形式总结出日常生活及工业生产中用于防锈的方法。
课上教学:
汇报、展示课题1的结果。
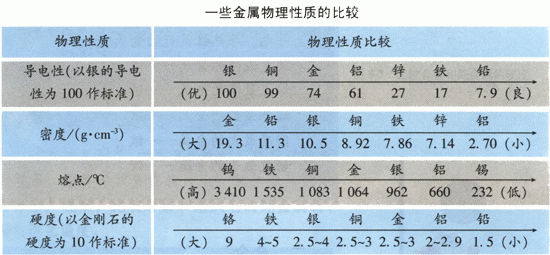
并思考:铁为什么会有这么多的用途?为什么我们用的菜刀、锤子等是用铁制的,而不是用铝制的?看下面的图,讨论。
(菜刀、锤子都应是由硬度大的物质做成,从表中可见,铁的硬度远远大于铝,所以,铁用有以上用途是因其硬度较大。学生也可能进一步提出问题:为什么不用铬呢?这里要讲解,在考虑物质的用途时,性质不是唯一决定因素,还需考虑价格、资源、美观、使用是否便利及是否易于回收和对环境的影响等多种因素。)
同理,铁的其它的用途在很大程度上也是由铁的性质决定。
那么铁到底有哪些重要的性质呢?
板书:一、 铁的物理性质
铁是我们生活中常见的金属,它具有一些多数金属共有的物理性质,比如:能导电,导热,常温下是固体等。此外,铁还有其自己的特性。
生活中见到的铁多不是纯铁,展示纯铁图片:

纯铁具有银白色的金属光泽,质软,有良好的延性和展性。密度是7.86克/厘米3,熔点是1535℃,沸点2750℃。铁是电和热的导体。

铁的用途不仅与物理性质有关,还和化学性质有关。比如铁为什么会生锈?为什么铁制的器皿不能盛装酸溶液?
板书:二、 铁的化学性质
观看录象:(铁生锈:1分29秒)
讨论课前铁生锈的实验:
展示: 一周前开始做的三个铁生锈对比实验结果。
分析思考:
1、三个实验的条件有什么不同?
2、三个实验的结果有什么不同?
3、这说明铁在什么条件下最容易生锈?
4、如何防止铁生锈?
5、举出你所知道的防止铁生锈的例子,它们的原理是什么?
小结:铁生锈是由于铁和氧气、还有水等物质作用发生的复杂的化学反应。
如果铁锈不除去,大家还会看到铁生锈的速度加快。这是因为铁锈很疏松,易吸水而加快生锈。
如何防锈?总结常见防锈方法。(视频)
启发: 铁锈的主要成份是什么?
是氧化铁( ![]() )。在氧气的化学性质学习中我们知道铁在氧气中点燃会发生剧烈的化学反应,生成产物是四氧化三铁。在这两种产物中,铁元素的化合价是不同的,三氧化二铁中显+3,四氧化三铁中铁显+2、+3价。为什么同一元素在不同的物质中会显示不同的化合价,即有这种变价现象呢?
)。在氧气的化学性质学习中我们知道铁在氧气中点燃会发生剧烈的化学反应,生成产物是四氧化三铁。在这两种产物中,铁元素的化合价是不同的,三氧化二铁中显+3,四氧化三铁中铁显+2、+3价。为什么同一元素在不同的物质中会显示不同的化合价,即有这种变价现象呢?
在排外电子排布知识学习中,我们知道元素的化学性质与其原子核外最外层电子排布关系密切。我们来看铁原子的核外电子排布。铁是26号元素:
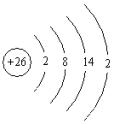

最外层有两个电子,处于不稳定状态,所以它易与氧化剂作用失去电子,当与弱氧化剂作用时,它只失去最外层2个电子,显+2;当与强氧化剂作用时,它还要失去次外层的1个电子,显+3。
铁是一种化学性质比较活泼的金属,如何去理解?
板书:1.铁与氧气的反应
由氧气的性质知,氧气可以与金属反应。如与镁、与铁。这两种金属与氧气反应有什么不同呢?仔细观察反应的现象,描述其反应现象。(观看镁在空气中燃烧、铁在氧气中燃烧的视频)
小结:镁与氧气更容易反应。
回忆以前学过的知识,金属除了可以和氧气反应外,还可与什么物质反应?(实验室制氢气的原理)
2.铁与酸反应
做铁与酸反应的实验,请学生描述实验现象。(生成物颜色、状态)并据实验现象写出反应方程式。
在氢气的制法中,我们知道某些金属与酸反应放出氢气。我们来做一组对比实验。
金属与酸的反应的实验:锌、镁、铁、铜与稀硫酸(稀盐酸)反应。(操作注意:加酸顺序从铜-铁-锌-镁)
提示学生要注意观察反应进行情况及放氢气的速度。
小结:镁与酸反应很快就有大量氢气泡放出,锌次之,铁更次之,而铜与酸不反应。由此,由上,镁的化学性质在以上四者中最活泼。铜最不活泼。
提问:以上几个反应,是属于基本反应类型中的哪一个?(置换反应)什么样的反应是置换反应?
3.铁与硫酸铜溶液的反应
演示实验:
观察现象:
提问:铜为什么不能置换铁?
小结:铁置换出了铜,因为铁的化学性质比铜活泼。置换反应发生的条件只能是化学性质活泼的单质置换出不活泼的单质。
通过以上铁与氧气、铁与酸、铁与硫酸铜溶液反应,表现出金属的性质。我们知道铁的化学活泼性比镁、锌弱,比铜活泼。金属活动性有顺序。看动画演示:
了解了铁的性质,我们就可以用于来指导实际的生活和生产。充分发挥有利的一面,而又最大限度的避免不利的一面。